2023年9月6日,埃默裏大學/中國科學院深圳先進技術研究院葉克強、華中科技大學王小川及江漢大學舒細記以共同通訊作者身份在 Nature Communications 發表題為 「Bacteroides Fragilis in the gut microbiomes of Alzheimer’s disease activates microglia and triggers pathogenesis in neuronal C/EBPβ transgenic mice」 的研究論文。該研究表明脆弱擬桿菌及其代謝物12-HHTrE和PGE2在神經元C/EBPβ基因改造小鼠中可啟用小膠質細胞並誘導AD發病。

01研究背景
艾爾茨海默病(Alzheimer’s disease ,AD)的兩個顯著特征是不溶性澱粉樣蛋白β(Aβ)沈積和磷酸化的富含Tau的神經原纖維纏結(NFT)。活化的小膠質細胞在大腦對神經元變性的免疫應答中起關鍵作用,小膠質細胞活化是AD發病機制的早期事件。腸道菌群失調是AD的發病機理之一,而在AD患者腸道微生物群中,擬桿菌菌株會選擇性地升高。然而,目前仍不清楚哪些擬桿菌物種及其代謝物如何引發AD的病理變化。
02結果
首先,為了探究AD腸道微生態失調是否能夠引發小鼠的AD樣病理變化,作者對正常野生型小鼠和Thy1-C/EBPβ基因改造小鼠持續兩個月灌胃AD患者和正常人的糞便,發現與接受健康供體糞菌移植(FMT)的小鼠相比,抗生素預處理的Thy1-C/EBPβ基因改造小鼠的AD患者糞便的再定植引起了AD病理(Fig. 1)。
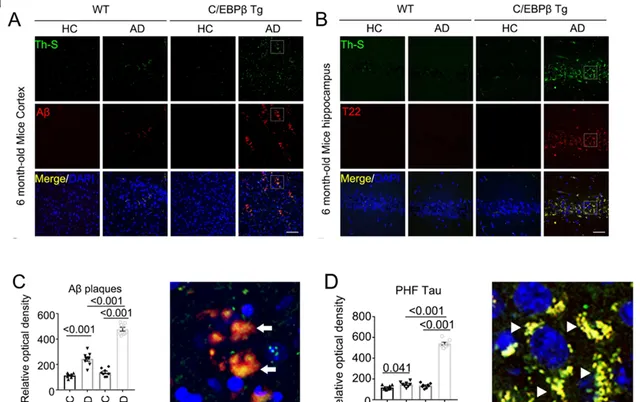
Fig.1 AD患者糞便移植在Thy1-C/EBPβ基因改造小鼠中誘導Aβ和Tau聚集
其次,作者評估了AD腸道微生物群引起的AD樣病理是否涉及C/EBPβ/AEP訊號啟用,發現AD腸道微生物引起C/EBPβ和其啟用狀態p-C/EBPβ均升高,然後引發AEP的上調,並造成小鼠認知功能障礙(Fig. 2)。
Fig.2 AD 患者的糞菌移植啟用了 C/EBPβ/AEP通路和基因改造小鼠的認知功能障礙
有研究表明C/EBPβ介導小膠質細胞調控炎癥和神經元細胞死亡,本研究發現AD糞菌移植後,正常小鼠以及基因改造小鼠海馬中陽性小膠質細胞的C/EBPβ訊號增強。包括IL-6和IL-1β在內的炎癥因子被AD患者腸道內的菌群啟用。AD的糞菌也上調了與多不飽和脂肪酸相關的代謝酶(Fig. 3)。
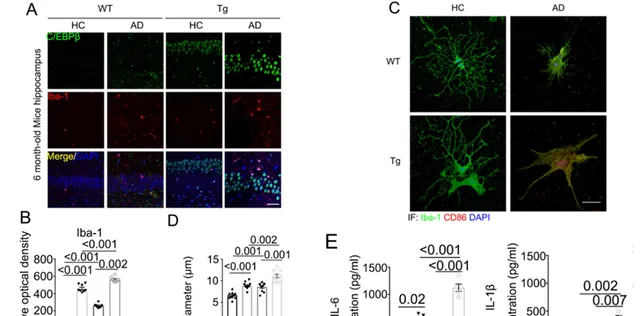
Fig.3 AD糞菌移植啟用小膠質細胞並增加Thy1-C/EBPβ基因改造小鼠的PUFA氧化酶
之前的研究透過微生物組和代謝組分析表明了脆弱擬桿菌可能在介導Thy1-C/EBPβ基因改造小鼠大腦中小膠質細胞活化和神經炎癥中發揮重要作用,為了驗證上述猜想,作者灌胃給予基因改造小鼠活的以及滅活的脆弱擬桿菌,發現活的脆弱擬桿菌引起Thy1-C/EBPβ基因改造小鼠中廣泛的病理性 Aβ 和 Tau 積累,同時還降低了小鼠的記憶認知功能(Fig. 4)。
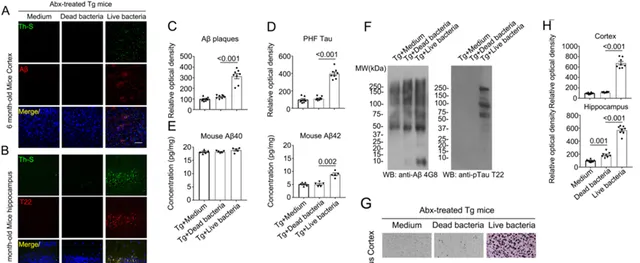
Fig.4 活的脆弱擬桿菌在Thy1-C/EBPβ基因改造小鼠中誘導AD樣病變
脆弱擬桿菌將花生四烯酸代謝為多種多不飽和脂肪酸衍生物,接下來作者為了探究這些代謝產物是否能夠引起AD樣病理變化,作者透過腹腔註射稀釋的12-羥基-十七碳三烯酸(12-HHTrE)或前列腺素E2(PGE2)溶液以5 mg/kg 的劑量每周兩次,持續4周。結果可以發現兩種代謝物都能引發海馬中Aβ蛋白和Tau蛋白的聚集並且誘發突觸變性以及損害認知功能,並且前列腺素E2在引發 AD 樣病理和認知缺陷方面表現出比 12-HHTrE 更強的作用(Fig. 5)。
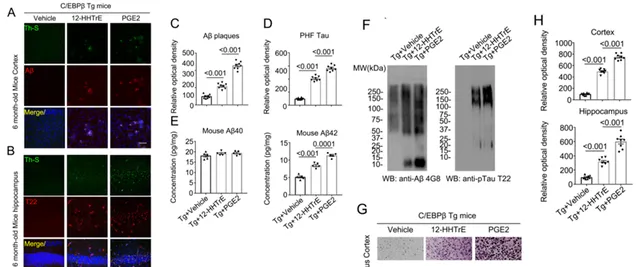
Fig.5 12-HHTrE或 PGE2 誘導Thy1-C/EBPβ基因改造小鼠的AD 樣病理和認知缺陷
03供稿者短評
在本研究中,脆弱擬桿菌及其代謝物12-羥基-十七碳三烯酸(12-HHTrE)和前列腺素E2(PGE2)在神經元C/EBPβ基因改造小鼠中啟用小膠質細胞並誘導AD發病。然而,該研究也存在著不足之處,給予AD患者糞便微生物的Thy1-C/EBPβ基因改造小鼠AD病理變化比正常小鼠嚴重的具體原因還需要進一步探究;其次,脆弱擬桿菌是否還存在其他代謝產物的變化同樣需進一步探究;再次,在尋找具體哪種代謝物質介導的AD病理變化以及小膠質細胞啟用,結合小鼠糞便、血清以及腦組織代謝組學,該項研究的框架會更為完整;最後,本研究只探究了大腦中C/EBPβ訊號的啟用,基於腸道到大腦傳播的「上行解剖理論」,可以進一步探討腸道中C/EBPβ訊號。
文獻來源
https://doi.org/10.1038/s41467-023-41283-w.2023.09.06











