(報告的出品方為興業證券)
【一、迎接常態化疫情防控與新醫改下的挑戰與機遇】
新冠疫情雖然已經被有效控制住了,可是疫情防控還是不能放松。
全國的疫情已經穩定下來,並且呈下降趨勢了。2022年開始,Omicron(Omicron)變異株讓國內的疫情防控又多了變數。Omicron(Omicron)變異株傳播速度快,還很隱匿,2021年底它先在歐美廣泛傳播開了,這就引發了全球新一輪的疫情爆發,咱們國家也面臨很大的「外防輸入」壓力。2022年上半年,國內多個地方出現疫情爆發情況,在堅持「動態清零」這個總方針的同時,防控措施也跟著時代發展不斷調整。因為各項防控措施都科學、精準地落實下去了,所以現在國內的疫情已經被有效地控制住了。國務院聯防聯控機制6月2日的新聞釋出會通報說,從5月30日開始,全國新增的本土感染者數量已經連續3天降到100例以下了,不過局部地區還是有小振幅的波動。國內疫情防控的整體形勢在變好,但是常態化防控可不能放松。
全球第四輪疫情已經開始走下坡路了。新冠Omicron變異株在2021年11月被首次發現,很快就在全球擴散開來,還引發了新的一輪疫情。從2022年1月疫情達到高峰之後,全球當天新增的病例數量已經大幅下降了。按照世界衛生組織(WHO)的統計數據,到2022年6月6日為止,全球累計報告了529,410,287例新冠確診病例,其中有6,296,771例死亡病例。自從1月26日達到高峰(單日新增確診病例為4,034,500例)以後,全球疫情總體上呈現出下降的趨勢。
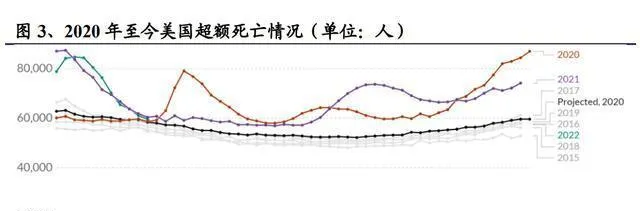
新冠疫情的影響在變小,要立足主業找下半年投資的主線。從2019年底發現首個已知新冠病毒感染者起,全球疫情讓各個國家和地區的經濟民生背負了沈重壓力。不過,在全人類共同努力下,防控檢測成了常態,新冠疫苗和藥物也從沒有到有了。在經歷Alpha、Beta、Gamma、Delta、Omicron等變異株的考驗後,防控措施和應對辦法也一直在「改進」。總的來說,新冠疫情的影響在逐漸變小。所以,展望2022年下半年,醫藥行業和疫情防控關系密切,這個行業的投資主線應該更多地企業「非新冠」的主營業務,布局行業裏的龍頭企業,挖掘有潛力的新企業。
1.2、政策的復盤和展望
1.2.1、藥品、高值耗材集中采購的復盤
總的來說,多輪國家組織、地區聯盟的采購一直在推進,集采的力度和深度都在不斷加強,集中采購常態化的局面已經形成了。以前幾輪集采積累了經驗,集采的競價規則、質素、供應、配送、使用保障機制和相關配套政策也越來越完善、最佳化了。在今年初國務院政策例行吹風會上,國家醫療保障局副局長陳金甫說,要接著推進集采速度加快、範圍擴大,爭取到2022年底,經過國家組織和省際聯盟采購,讓每個省平均覆蓋350個以上的藥品品種。以後國家、省際的集中采購還是會有秩序地推進,覆蓋更多需求量大、金額高的藥品品種。
不光是藥品,高值醫用耗材也在透過國家組織、地區聯盟以及各省市帶量采購的形式不斷快速推進。現在高耗集采主要牽涉心血管介入、眼科、骨科這些領域,在大幅降價的同時,覆蓋範圍越來越大,品類也越來越多,相關的規則政策也越來越完善。從長遠看,耗材帶量采購對提升行業集中度有好處,將來在政策的推動下,有望采用更多樣的聯盟采購方式、更細致的評價競價機制,覆蓋更多臨床需求大的醫用耗材,從而推動國產產品替代進口產品,鼓勵創新,推動產業結構升級。就拿近期推出的骨科脊柱類耗材采購來說,按照【國家組織脊柱類醫用耗材集中帶領采購方案(征求意見稿)】,這次集采依據手術類別、手術部位、入路方式等區分元件產品系統,然後按系統進行采購,總共包含13個產品系統、8種材質,把不低於醫療機構填報需求量的80%當作意向采購量,綜合考慮醫療機構需求、企業供應能力等多方面因素進行多單元競價。這一輪的國家集采也許會改變之前國內脊柱高值耗材由外資品牌占主導的狀況,質優價廉的國產品牌有望借此進一步拓展市場。
1.2.2、DRG/DIP和相關重點政策:改革進入快車道,新管理方式推動供給側結構性改革加速。
中國醫藥衛生體制改革重點清晰。2022年重點工作任務依舊圍繞這些方面展開:全面推進健康中國建設,深入推廣三明醫改經驗,推動優質醫療資源擴容並均衡布局,深化醫療、醫保、醫藥聯動改革,不斷促使從治病為中心向以人民健康為中心轉變,持續解決看病難、看病貴的問題。DRG/DIP呢,它是衡量醫療服務質素與效率、進行醫保支付的精細化管理工具,能讓醫療服務的透明度進一步提高,促使醫療費用及其結構更合理,對分級診療也有促進作用。
DRG/DIP醫保支付:新支付方式助力醫院降本增效。醫保支付機制改革之後,醫院采用多元復合的支付方式,不再單獨給各個醫院設定醫保報銷總額的上限了。而是以醫保基金區域總額預算為基礎,對不同疾病和部門采用多種支付方式,像急性住院治療按疾病診斷相關分組(DRG)/按病種分值(DIP)付費、部份長期住院治療按床日付費、基層門診和部份慢病按人頭付費、門診和不適合打包付費的病例按專案付費。在新支付方式下,針對急性住院治療的DRG/DIP實行「預付制」支付方式,就是醫保先預付一筆費用,醫院要在醫保給定的費用額度裏控制支出,住院醫療時的治療專案從醫院的「收入」變成了「成本」。同時,收治患者多、患者疾病嚴重程度高的醫院會得到更多醫保額度,這在合理分配醫療資源的同時能促使醫院降本增效。
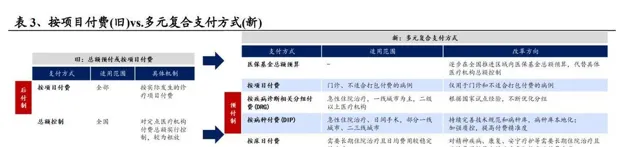
具體而言,DRG/DIP采用的是區域總額預算下「結余留用,超支不補」(DRG)或者「結余留用,超支合理分擔」(DIP)這種預付制支付方式。這樣一來,就促使醫院從追求服務量轉變為追求醫療質素和管控成本,進而推動合理診療,更好地實作醫療價值。醫療機構在經營管理上得更看重成本效益了,醫療決策者在挑選藥品、耗材、檢查檢驗手段和治療方法的時候,也會充分考量效價比。和「按專案付費」比起來,DRG/DIP激勵醫院把治療專案和成本控制在合理範圍;和「總額預付」比起來,DRG/DIP激勵醫院提升效率,收治更多患者。
【中國醫療保險】有統計,到「十三五」結束的時候,DRG/DIP支付方式差不多覆蓋了36.5%的參保人口,這裏面DIP的覆蓋範圍更大些。到2021年12月,全國71個試點城市總共覆蓋了大概3.19億參保人員,占全國參保總人數的23.4%左右。咱們國家各個統籌區算DRG/DIP醫保該支付的費用方法不一樣,自費部份是不是算進去,各地政策有點差別。現在,各地DRG/DIP醫保基金支付的計算方法還沒統一呢。國家醫保局發的DRG技術規範裏說,算DRG醫保基金該支付的費用時得把患者自費部份考慮進去。按照這個演算法,在同一個DRG組的支付標準下,理論上講,患者治療時自費費用越高,醫保給醫院的錢就會越少,所以醫院可能就會主動減少治療中的自費專案。不過,各地實際操作的時候,有些統籌區的醫保基金和醫院結算時並沒有考慮患者自費的部份。
2009年的時候,國務院醫改領導小組辦公室發了個【關於公立醫院改革試點城市申報工作通知】。打那以後,各個試點城市的公立醫院就慢慢取消藥品加成了,住院藥占比也一直在下降。到2017年9月底,全國公立醫院都實作了「藥品零加成」。2019年住院藥品費用占比降到了27.5%,和2010年的43.1%比起來,少了不少呢。醫院藥占比以後可能還會降。DRG/DIP實施之後,醫院為了降成本,可能會主動少用藥。那些沒在臨床路徑裏的藥,進醫院就更難了。住院部用藥可能會優先選性價比高的產品,這樣一來,醫院藥占比有望進一步降低。住院檢查檢驗可能會慢慢在醫院內部的部門之間轉移。在DRG/DIP推行之前,住院檢查檢驗費用占比是逐年上升的,2020年大概是10%。參考國外的經驗,在門診費用精細化管理措施推行之前,在DRG/DIP的成本控制下,部份住院檢查檢驗可能會轉到門診那邊去。

中國住院手術費在住院醫療總費用裏占的比例,比海外那些醫療體系比較成熟的國家低很多呢。2019年的時候,中國住院手術費占比還不到8%。德國也有社會醫療保險制度,同一年,德國住院手術相關費用占比能達到70%這麽高。所以啊,估計中國住院醫療費用裏人工費用占的比例還會進一步提高。新醫改開始以後,中國已經接連出台了不少關於公立醫院薪酬制度改革的指導意見。等DRG/DIP和其他醫改政策都實施以後,預計醫院住院費用的結構會更加朝著醫療服務的核心價值部份傾斜。
DRG/DIP和集采是相輔相成的,不過它們各有重點。集采實行之後,像部份藥品、醫用耗材這些產品的價格就降下來了,這樣一來,醫院在執行DRG/DIP的時候,在控制成本、挑選性價比更高的產品時就有了更多的選擇空間。但是呢,DRG/DIP和集采政策在功能定位上並不完全一樣。DRG/DIP重點是借助精細化管理讓醫療費用更合理、費用結構更合理,透過設定科學合理的疾病分組和付費制度來促使醫療資源分配得更合理;集采則更著重於讓產品價格合理,解決產品價格過高,還有流通秩序、銷售行為裏可能存在的不規範問題。
總結:DRGs在國外發展超半個世紀了,這是個提升醫院服務透明度、衡量醫療服務質素和效率,還有用於醫保支付的重要工具。DIP是從DRG衍生出來的,是符合咱們國家國情的本土化醫院管理和醫保支付方式。在管理上,DRG/DIP會把臨床治療和資源消耗相近的病例歸到同一個病組,這樣醫院管理起來方便,醫療行為也能測量和評估;在付費方面,醫保基金能按照DRG/DIP同病組可比費用的標準給醫院付費。DRG/DIP不是單獨的政策體系,把它和醫藥分家、藥耗集采、醫療服務價格改革這些相關政策結合起來,有望一起推動新醫改目標達成。
1.3、對各細分板塊走勢進行復盤
從年初到現在,各個醫藥細分板塊都有不同程度的調整。這大概和國內多地疫情散發、俄烏沖突這些國內外宏觀方面的變化影響了市場信心等因素有關。年初到2022年6月2日為止,醫藥生物(申萬)板塊整體跌了24.09%,全部A股跌了13.48%,醫藥生物(申萬)比全部A股多跌了10.61%。在各個細分板塊裏,醫藥流通(申萬)的走勢相對來說比較好,只跌了9.67%,主要是因為醫藥流通(申萬)板塊在醫藥各細分板塊裏估值相對低,避險的特性很明顯;但是疫苗(申萬)和研發外包服務(申萬)上半年走勢就比較差,分別跌了36.89%和33.55%。這裏面,疫苗(申萬)板塊調整的振幅很大,大概是HPV疫苗等行業新聞影響了市場情緒的緣故,研發外包服務(申萬)板塊大幅調整,大概是和市場擔心地緣政治、創新藥的景氣程度等因素有關。
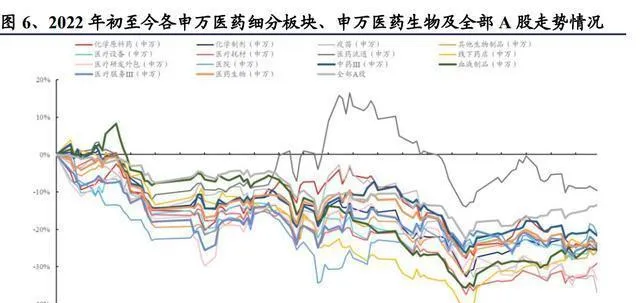
2.1.1. 醫療服務方面:門診修復的速度比住院快,眼科產業鏈的景氣程度較高。
從醫院的數據統計來看,疫情結束之後,2021年醫院的門診量已經比2019年的水平還高了,不過住院量還在恢復當中。為啥會這樣呢?大概是因為在疫情常態化防控的時候,那些需要擇期治療的患者把需求往後推了,還有異地就醫住院的患者需求也變少了。往下半年看的話,估計門診和日間手術需求的恢復速度還是有可能比住院類專案要快。
眼科近視防控賽道因為滲透率提高和新產品推出,成長性更強了,行業一直很景氣。衛健委的調查數據表明:2020年中國兒童青少年總體近視率是52.7%,跟2019年比上升了2.5個百分點,和2018年比下降了0.9個百分點;6歲兒童近視率為14.3%,小學生是35.6%,初中生71.1%,高中生80.5%。近視防控的需求比較固定,角膜塑形鏡和離焦鏡的滲透率都不到2%,低濃度阿托品的院內制劑使用也比較受限,以後供給側渠道往下發展和防控手段變多,有望讓這個行業一直快速增長。

2.1.2. 連鎖藥店:經營的節奏恢復了,龍頭藥店加快擴張。
連鎖藥店從今年開始慢慢回到正常的經營節奏了,在疫情期間就表現出很強的韌性。4月的社會消費品零售數據公布了,中西藥類的零售總額達到505億元,跟去年同期比增長了7.9%,這個增速在各類商品零售細分裏排第二呢;1到4月中西藥累計的零售額是1990億,同比增長8.8%,這就顯示出很強的防禦性了。
行業增長主要還是靠處方外流和集中度提高,龍頭連鎖藥店以後增長的空間很大。2021年的時候,那些頭部連鎖藥店的集中度又有了進一步的提高,CR10的市場占有率提高到了27.56%。2021年,零售藥店終端藥品銷售占的比例達到了26.9%,預計2022年的時候,隨著雙鍊結政策落地,院外渠道的價值會更加凸顯出來。
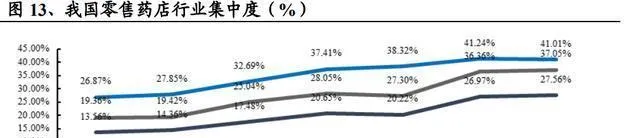
2.2、中藥消費品和品牌OTC,歷經大浪淘沙才見真金。
長遠看,中藥消費品和品牌OTC行業的發展趨勢很不錯。政策方面,這個行業能從中藥行業的政策扶持和多數品類自費的特性中受益,有一定的避險能力;需求方面,由於消費升級,渠道和消費者都更看重品牌了,這就使企業的品牌價值提高,行業形勢向好。在這當中,品牌OTC這個領域發展得比較成熟,不過隨著品牌價值提升改變了行業格局,那些有核心品牌影響力的品牌OTC行業的龍頭企業有望得到結構性的機會;中藥消費品領域更能直接地從消費升級帶來的需求增長中受益,而且在供給方面能享受稀缺性和品牌價值帶來的好處,有持續提價的能力,有望實作量價一起增長的發展機會,其中品牌價值高、有優質核心產品,並且在銷售、渠道、管理方面都不差的企業有望保持穩步增長的態勢。
2.2.2 短期發展趨勢向好:政策環境有利,結構方面的變化對龍頭企業是個利好。
政策的避險內容變得很明顯,再加上OTC品種大多是自費支付的,所以自主定價的能力比較強。政策對中藥行業的發展是支持的,中藥消費品和中藥OTC在這種友好的行業環境裏受益。2021年開始,中醫藥相關的政策落地速度加快了。2022年3月,國務院辦公廳印發了【「十四五」中醫藥發展規劃】。和之前國家中醫藥管理局印發的【中醫藥發展「十三五」規劃】比起來,能看出來中醫藥的發展被定位得更高了,也受到了更高層級的重視。
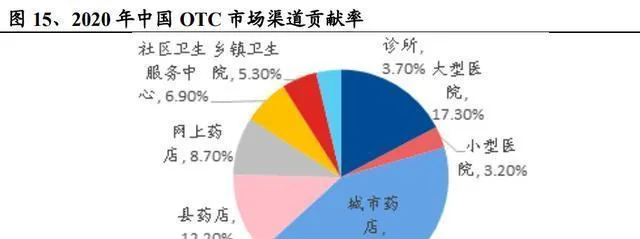
OTC藥品主要在院外銷售,集采風險不高,自主定價能力應該能保持。零售藥店和互聯網渠道是OTC產品很重要的銷售終端,大多是自費購買。IQVIA的數據顯示,OTC藥品銷售渠道裏,城市藥店和縣藥店的銷售額加起來占54.9%,網上藥店占8.7%,這三個院外渠道總共占63.6%。所以,預計它受醫保控費和集中采購的影響比較小,自主定價能力更強。
OTC企業的渠道變革和去庫存都慢慢弄完了,渠道管理能力大多都提高了。醫藥流通渠道越來越規範,一些OTC企業進行了行銷體制改革,也清理了渠道庫存。在渠道變革完成之際,OTC企業還用資訊化建設、藥品追溯碼體系這些辦法提高了渠道和終端庫存的管理能力,庫存周期沒那麽明顯了,有些企業的存貨周轉天數還變少了。
成本上漲推動,再加上需求端對價格的接受度比較高,開始進入新的一輪提價周期了。
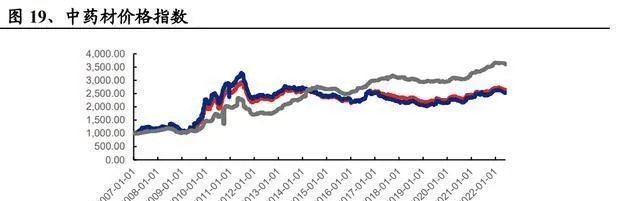
中成藥上遊的原材料一直在漲價,成本增加是提價的關鍵催化因素。2021年到2022年3月,中藥材價格漲了超過11%,野生品種指數漲得更多,達到13%;還有天然牛黃,它比較稀缺,在2019年12月到2020年12月這一年裏,價格漲了21%。
居民收入和醫藥消費品價格有個「剪刀差」,這使得醫藥消費品需求進一步增加。大部份醫藥消費品價格調整的振幅,比居民收入增長水平小,醫藥消費品提價時,需求端的購買力是能支持的。拿高端醫藥消費品同仁堂的安宮牛黃丸來說,2010年到現在,它一共三次公開提高終端銷售價,累計漲價振幅是146%,這個振幅比人均可支配收入的累計漲幅要低。
一些品牌的OTC和中藥消費品,靠著強大的品牌影響力,在成本上升的推動下一個個都提價了,這就促使業績增長。其中有些中藥消費品因為具有稀缺性,競爭態勢更好,提價的時候也更靈活。2021年12月同仁堂給安宮牛黃丸提價之後,很多中藥消費品企業也陸續給部份產品提價了,那些有較強自主定價能力的品牌OTC企業也有調價的情況。
國企透過改革、把治理理順、激勵做到位,管理得到改善後,就會進入發展的新階段。
2021年到現在,有一部份中藥行業和OTC(非處方藥)的公司,在管理方面有很明顯的積極變化。這裏面有不少是傳統企業,它們已經受益或者可能受益於國企改革浪潮,也許會在改革過程中增添新的發展活力。目前管理方面的變化主要有兩點:一是像實際控制人改變或者管理層調整這種情況,這意味著企業進入了新的發展階段,在新的體系和治理模式下,有望實作資源整合、提升管理效率等新的發展動力;二是透過股權激勵、員工持股計劃、對核心子公司進行激勵等不同激勵方式,來增強企業發展的動力。(報告來源:未來智庫)
對於整個醫藥大行業來說,「創新+消費升級」是投資邏輯,對疫苗這個小行業而言,它也是發展的推動力。行業的供需結構有了變化之後,國產疫苗,特別是國產二類苗,安全性、保護效力與範圍一直在提高。不管是包裝從西林瓶變成預灌封,還是工藝從Vero細胞升級到二倍體細胞,又或者是產品從多糖升級到多糖結合、從單苗變成聯苗、從單價變為多價,消費者自費的創新二類苗通常定價權更強。並且,隨著中國人均可支配收入和公眾健康意識普遍提高,二類苗的滲透率也可能進一步提高。有創新能力的國產疫苗企業也許會迎來「量價齊升」的好行情。同時,中國也會慢慢從「疫苗大國」轉變成「疫苗強國」。
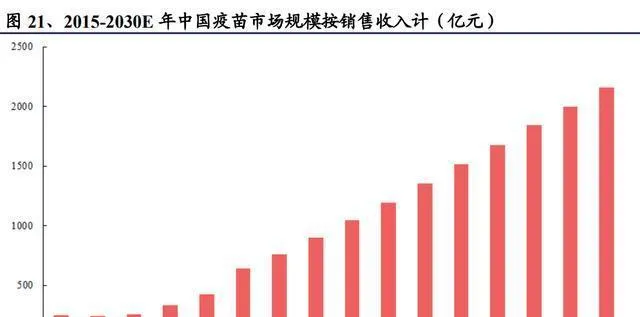
需求端方面,公眾健康意識提高了,這有望讓二類苗的滲透率加快提升。疫苗滲透率會隨著經濟發展一塊兒提高,偶爾發生的事件可能會使接種率短期內有波動,但不會影響長期的發展走向。公眾對疫苗的安全性、保護能力以及依從性的要求一直在提高,這會進一步促使企業去研發,給行業發展指明方向。疫苗經過幾百年的科學驗證和經驗積累,在預防疾病和根除傳染病上起著非常關鍵的作用。人類以前靠疫苗根除了天花;也有過因為「疫苗猶豫」而不接種百白破疫苗,結果好幾萬兒童得了百日咳。不過疫苗確實存在著一些無法避免的問題,像不良反應風險、保護效力有限,還有些疾病領域很難攻克,這些都得依靠技術不斷進步、產品不斷升級才行。國內外的疫苗研發企業也一直在為人類的疾病免疫事業努力。新冠疫苗廣泛使用,有望讓公眾的接種意識增強,向成年人全面普及疫苗接種知識,使疫苗接種資訊更容易獲取。中國疫苗市場的重點正從嬰幼兒慢慢轉向成年人,二類苗的滲透率有望持續提高。
【三、把握供給升級下的創新紅利與工程師紅利】
3.1、生命科學的上遊發展進入新階段了,頭部的公司優勢慢慢凸顯出來了。
中國生命科學的上遊行業發展得很蓬勃。
生命科學上遊產業鏈,就是給生命科學研究和生產(像生物制藥、體外診斷這些)的整個過程提供服務的相關產業,這裏面有相關的儀器器材、耗材、原料,還有服務,它可是生命科學行業發展的關鍵基礎設施。生物醫藥這一塊發展特別快,新技術一個接一個地冒出來。在研究的時候,像靶點發現、靶點選擇、抗原制備、候選藥物篩選和功能鑒定這些步驟,對生物試劑、耗材和試驗用的儀器器材都有很大的需求量。生物藥的工藝開發和生產又復雜又麻煩,還特別專業,像培養基配制、種子培養、規模放大、發酵生產、分離、純化、過濾和灌裝這些環節,也得有大量專業的儀器器材、原料以及耗材來支持才行。
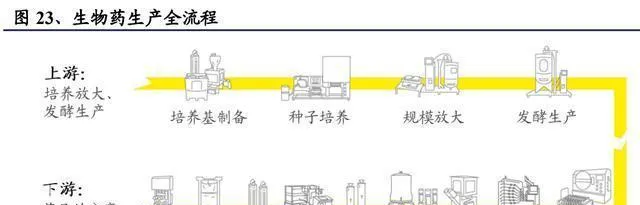
下遊生物制藥行業需求不斷增長,這就帶動著相關行業一起快速發展。預計在接下來的幾年裏,生物藥上市會迎來高峰期。那與之相配套的生命科學支持產業,也很可能快速發展起來。整個行業一直處在快速發展的狀態,以後的發展空間非常大。
生命科學上遊的主要標的,其估值處在歷史上相對低的位置。
醫藥上遊產業鏈這近一年來調整了挺長時間。總結一些上市兩年以內的生命科學上遊公司的估值情況就能發現,上遊行業的估值和一年前比已經回落了些。上市還不到一年的次新股也經歷了估值調整。市值調整了,上遊公司業績又高速增長,這兩個因素讓上遊行業估值的中樞整體明顯下移了,不過還是比醫藥行業的總體估值水平要高。
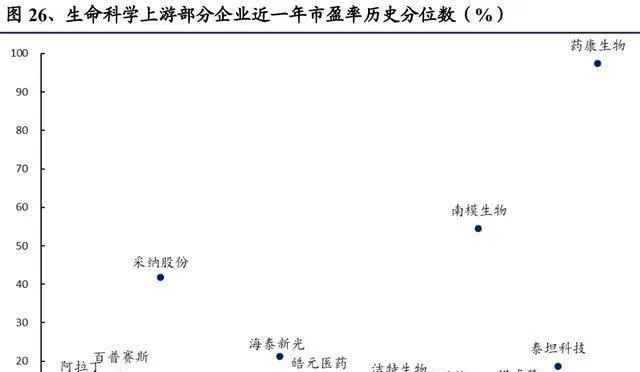
2022年上半年,國內疫情反復,這對生命科學上遊行業裏部份公司4 - 5月的經營可能有一定影響。有些企業是供給端受影響,還有些企業則是需求端(像高校、科研院所和藥企這些)受影響。不過,隨著之後國內疫情形勢預計會逐漸變好,就會發現,2020年第二季度,大部份代表公司的營收環比增速明顯上升了,比2021年第二季度的環比增速快不少,這就表明2020年第二季度業績增長得比較快,不是僅僅因為公司經營在季度之間有波動造成的。我們分析,2020年第二季度業績環比增速大幅提高,主要是因為疫情之後有「需求回補」。生命科學上遊和科研服務的產品,在醫藥研發、生產裏算是比較剛需的產品。疫情緩和之後,高校和科研院所的客戶要趕著做課題(畢業時間和基金結題時間是固定的),企業客戶要加班完成預定的研發和生產任務,這些都可能把原本在疫情期間該有的產品需求補回來,這樣業績就反彈了。
中長期的話,比較看好那些能夠做到跨領域發展,還能走向國際化的行業裏的龍頭企業。
生命科學的上遊產業這近兩年發展得特別快,在收入、利潤和公司規模方面都有不小的提升,還有很多公司順利完成首次公開募股(IPO),進入到二級市場了。現在國內的公司正在生命科學產業的各個環節努力,差不多已經把整個產業鏈都覆蓋到了。

跨領域能力是行業領先企業實作長遠發展的必要條件。中國生命科學上遊行業整體起步較晚,現在行業裏的公司大多是專註於單一細分領域的「小龍頭」企業。在生命科學行業,產業鏈又長又復雜,客戶需求各式各樣,所以完備的產業能力和齊全的SKU種類是這個行業很重要的有利競爭。細分行業包含機械、材料、生物等多個不同領域,技術壁壘比較高,通常得長時間積累技術和品牌。企業一般很難在短期內光靠自己研發就突破其他子行業的技術難關。像國際龍頭企業Thermo Fisher就是不斷並購,才具備了橫跨生物制藥、診斷、分析儀器、實驗室產品和服務等多個領域的能力,而且還在持續並購以增強在細分市場的影響力。
國內的上遊企業也都在積極拓寬自身能力範圍。就目前的情況而言,多數企業從自身業務入手,漸漸朝著與現有業務相關領域的其他方向拓展。比如納微科技以純化填料為基點,打算收購生產蛋白純化儀器的賽譜儀器,達成在蛋白純化方面器材和耗材的協同。諾唯贊已經成立了好幾個子公司,在實驗耗材、儀器器材等多個領域進行探索。產業裏也有積極進行跨領域布局的公司。東富龍在2021年收購了填料企業千純生物51%的股權,還投資了過濾企業杭州賽普(持股25%),並且在培養基領域組建團隊進行布局。多寧早在2020年就完成了對亮黑科技的並購,從而成為在一次性耗材、生物反應器、培養基方面都有相關業務的企業;2022年3月,多寧接連並購樂楓生物和SALUS,把產品矩陣擴充套件到了實驗室水純化領域。
參照國際上那些龍頭企業的發展經驗來看,跨領域發展對企業以後不斷發展、變得強大,構建起自己的護城河來說,是必須要走的路。在中國生命科學上遊行業的各個細分領域裏,那些頭部公司經過這兩年的發展,在資金規模、融資途徑、行業裏的地位等方面,和後來者比起來都有一定的領先優勢。所以我們覺得,要是走並購跨領域發展這條路,各個細分領域的龍頭企業優勢很明顯,以後更有機會透過整合成為行業裏的老大。國際化是那種只做單一產品的公司的另一個發展方向。因為單個細分領域的市場空間比較小,一個國家或者地區的需求相對而言是有限的,只做單一產品的企業很難發展成規模很大的公司,所以那些沒能力進行跨領域發展的公司就得找另外一條路,來打破市場規模的限制。中國大多數生命科學上遊公司在海外的收入數額比較小,但是在全球生命科學上遊的各個細分領域,像生物試劑、培養基、純化填料這些領域,市場規模都比國內大很多,有非常大的挖掘潛力,所以國際化自然就成了單一產品型公司以後需要大力發展的方向之一。
抓住技術變革的新契機。
國產企業在生物技術新領域有趕超的機會。傳統領域裏,國產企業在基礎能力和生態體系建設方面還有很多需要提升的地方。每次有突破性的新生物技術或者新療法出現,都會極大地影響全球醫藥產業的競爭格局。就像最近mRNA疫苗技術快速發展,全球醫藥市場上出現了Moderna、BioNtech和CuerVac這些新崛起的企業,國內也有艾博生物、斯微生物等一批迅速發展起來的公司。
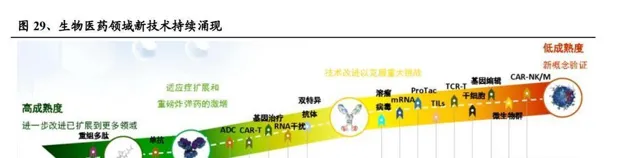
新技術也催生了新工藝路線和新相關產品的需求。全球的生命科學上遊企業,針對新技術路線做產品研發和探索基本沒有捷徑。像新興的細胞和基因治療領域發展起來後,上遊生產中對病毒載體和質體的需求增大了。這一領域發展的時間短,所以國產公司能參與到最前沿的研究中,在新產品領域和傳統巨頭處在同一起跑線。在生物創新藥發展的浪潮下,中國生命科學上遊領域的公司有了第一次快速的發展和積累。在新技術不斷湧現的時代,中國生命科學產業及其上遊都要面臨後續的變革,並且積極參與到相關技術革新的大潮裏。
3.2、CXO賽道的景氣度仍然還在。
來復盤一下2021年起CXO板塊的走勢(就以CRO指數(8841421.WI)為代表吧)。從2021年10月開始,這個板塊就進入下行周期了。最開始,估計是投融資數據每個月的波動引發的,後來呢,像行業自身的一些情況、板塊的估值、新冠藥物訂單、行業的景氣程度這些,都成了持續影響CXO板塊的重要因素。現在呢,我們覺得這些影響因素經過之前的消化,對板塊的壓制在逐漸減輕,要是碰到一些緩和的訊號,就有可能讓板塊向上發展。並且,之前板塊下跌把估值溢價消化了不少,現在CXO板塊的估值處於比較低的水平了。就目前旺盛的訂單需求,還有產能快速擴張的趨勢來看,CXO在醫藥板塊裏仍然是業績確定性比較高、成長性比較強的賽道之一。
藥企的研發投入剛需是CXO行業的核心驅動力。
從投融資數據方面看,回顧海外市場的情況,海外部份CXO公司和納斯達克指數2000年之後每年的收益率就會發現,在美聯儲緊縮期間,大部份年份裏海外CXO公司的平均收益率都明顯比納斯達克指數高,不過在2008年金融危機以及之後的3年裏,海外CXO公司的收益率就比不上納斯達克指數了。所以我們認為,要是沒有重大金融事件擾亂全球市場的話,海外流動性收緊(美聯儲收緊)對CXO公司的業績和股價表現並沒有產生很大的負面影響。
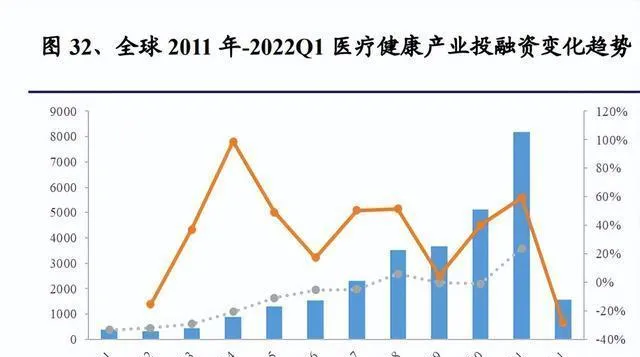
把投融資數據復盤一下就會發現,2020年和2021年的時候,全球和國內的醫療健康產業融資金額都增長得特別快。2021年全球的同比增速差不多是59.5%,國內的同比增速大概是38.8%。這對中國中短期內CXO公司的訂單來源以及業績增長來說,是很強有力的支撐。到了2022年,投融資數據就有了一定的波動。2022年第一季度因為2 - 3月的數據影響,全球融資金額同比下降了大概29%,國內融資金額同比下降了差不多34%。4月的數據還是接著2 - 3月的下降趨勢。
2022年,國內外投融資的數據不太好,不過估計這對行業裏的龍頭企業影響不大。我們覺得這裏面有美股biotech估值下降、國內創新環境變嚴等原因,也有醫藥產業投融資有周期,去年同期基數比較高的因素。短期內,全球醫藥行業投融資數據可能還會被壓制,2022年下半年的投融資情況還得接著觀察。對於biotech而言,融資後持續投入研發是它自身發展的主要動力,再考慮到融資後賬上現金的使用周期,產業投融資數據確實可能會有一定周期波動。總的來講,現在投融資數據的波動暫時沒有影響到中國CXO行業的訂單和業績增長,以後雖然不能排除會有影響,但估計影響比較小,對行業龍頭的影響就更小了。
另外,在投融資之外,big pharma的研發費用是創新研發資金的「基本盤」,它的穩定增長也是CXO能保持景氣的重要動力。回顧歷史就會發現,big pharma的營收大體上是穩定增長的。雖說全球新藥研發的難度一直在增加,但是研發費用率整體是穩步上升的。從研發費用這方面來看,2013年之後,big pharma的研發費用又整體開始增長了。
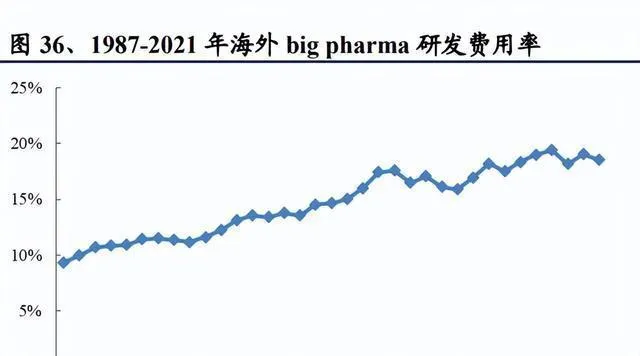
中國小分子CDMO產業的發展趨勢是可持續的。
這幾年,多數制藥企業都在削減歐美那邊的研發和生產業務,越來越多的藥企把生產外包業務往亞洲這邊轉。從全球創新藥的發展情況來講,鑒於CDMO滲透率還會持續上升,我們覺得全球市場對CDMO訂單需求總量大體上會保持穩定增長的態勢。因為需求一直在增長,從中國小分子CDMO行業的發展空間來看,按照藥明康德公布的數據,到2021年上半年的時候,藥明康德CDMO管線裏處於臨床階段的創新小分子藥物數量,在全球市場裏已經占了大概14%的份額。要是把凱萊英、博騰股份、九洲藥業等國內CDMO頭部企業的專案數量也算上的話,根據我們大致的估算和測算,到2021年上半年,國內CDMO企業管線裏處於臨床階段的創新小分子藥物數量在全球市場裏所占的份額已經超過25%了。總的來說,從專案數量上看,目前中國CDMO行業在全球小分子CDMO市場已經占了很重要的位置,不過還有上升的空間。
CXO這個行業的發展趨勢一直是向好的。
對CXO公司來講,產能和訂單是衡量公司與行業景氣程度的關鍵指標。公司對未來幾年行業景氣狀況以及自身訂單增量情況的判斷,決定了產能的擴增計劃。要是產能利用率一直處在高位,那麽擴增產能就是業績增長的重要因素。訂單呢,是公司保持較高產能利用率的保障,也能更好地為後續發展趨勢指明方向。在CDMO公司或者相關業務裏,生產基地的投入是重中之重。隨著產業轉移速度加快,各個公司的產能或者在建工程都增長得比較快。同時,各個公司的資本支出也漲得很快,為產能的快速增長提供了保障。拿藥明康德來說,2021年公司的資本支出是69.36億元,和上一年比增長了128.84%。根據2022年一季報,2022年公司有望投入90 - 100億的資本支出,公司的產能建設仍然保持加速狀態。另外,從反應釜體積這個角度看,以凱萊英為例,它的產能釋放也在加速。到2021年底,公司傳統批次反應釜體積接近4700m3,公司預計到2022年底,小分子傳統批次反應釜產能和2021年底比將增長46%。藥石科技承擔主要生產任務的子公司浙江暉石的501車間在2022年成功投產,產能增長了90%,502和503車間也處在建設的關鍵時期,這就有了較大的產能彈性,有希望突破產能瓶頸,重新走上快速增長的道路。
臨床前和臨床CRO業務的產能,關鍵在於相關人員的數量。2021年呢,那些以臨床前或者臨床CRO業務為主,或者有相關業務的主要公司,人員數量都增長得比較快。比如說,到2021年底的時候,藥明康德的員工總數達到了34912人,和上一年比增長了32.2%;康龍化成在2021年底做實驗室業務的員工有7136人,同比增長28.4%;泰格醫藥的員工數從2020年末的6032人增加到2021年末的8326人,同比增長38.0%;美迪西在2021年搞藥物發現板塊的研發人員有1067人,同比增長58.31%,藥學研究板塊的研發人員有326人,同比增長29.37%。從各個公司公布的在手訂單或者新增訂單來看,每家公司的訂單也都保持著較快的增長勢頭,這就表明這個行業現在的景氣程度比較高。泰格醫藥2021年新簽的訂單是96.46億元,同比增長74.2%,2022年1 - 2月在手訂單同比增長超過65%;美迪西2021年新簽的訂單是24.52億元,同比增長87.66%;昭衍新藥2021年簽的訂單超過28億元,其中在國內承接的訂單金額超過25.5億元,同比增長大概65%。同時呢,大訂單也促使不少公司的業績增長了,像凱萊英簽的重大【供貨合約】,訂單合約金額累計是4.81億美元 + 27.20億人民幣 + 35.42億人民幣,到2021年年報披露的時候,公司在手訂單總額是18.98億美元(和上一年比增長320%);博騰股份累計拿到了8.98億美元的重大合約等。(報告來源:未來智庫)
3.3、創新藥的創新速度依舊不減,差異化、商業化和國際化仍然是重點。
3.3.1、對創新藥全板塊的分析
創新藥是個啥概念呢?
最開始的時候,對於「創新藥」的定義有很多不一樣的看法。監管機構從研發者的角度考慮,中間也修改過好幾次。一直到2021年7月2日,CDE(藥品審評中心)釋出了一個檔,叫【以臨床價值為導向的抗腫瘤藥物臨床研發指導原則】征求稿,這個檔頭一回明確地說,創新藥得「落實以臨床價值為導向,以患者為核心的研發理念」。和之前的那幾次定義比起來,這次提出來的概念更多地從臨床價值、患者利益,甚至社會價值這些方面去判斷創新性了。
國際化(liscence out)恰逢其時。
在歐美已開發國家的市場裏,Big pharm和Biotech之間進行成果交易已經是一種常見的行為了,這種交易一起讓整個醫藥行業的創新氛圍得以良好地保持運轉。Big pharma把Biotech的成果引進來,讓自己的管線更充實,再憑借很強的商業化能力,讓新藥快速上市並且產量不斷增加;Biotech把自己產品的權利授權出去,就不用經歷漫長又不確定的商業化開發過程了,還能很快得到很多的研發回報,好投入到下一次研發當中。
創新藥研發經驗不斷積累後,有差異化和「Best - in - class」潛力的創新藥專案更容易被海外藥企看上。不完全統計顯示,2020年到2022年1月底,中國藥企和境外藥企簽的合作開發、權益轉讓協定有50多項已經完成。這裏面首付款最高的是百濟神州和諾華簽的關於PD - 1抗體百澤安在好多國家(像美國、加拿大、歐盟成員國等)開發、生產和商業化的合作協定,首付款達到6.5億美元。榮昌生物的ADC藥物維迪西妥單抗跟Seagen簽協定,總轉讓金額達到26億美元,重新整理了紀錄。良好的合作關系以及管線之間的協同,對後續研發產品的轉讓合作有幫助,百濟神州和君實分別跟自己PD - 1單抗轉讓交易的合作方簽了TIGIT單抗的轉讓權益。各個轉讓協定的首付款或者交易總額差別很大,這主要和專案的合作時間點以及潛在的商業化價值有關。對於獲批風險高、非常早期的合作(像臨床前專案),首付款常常在1億美元以下;而對於商業化價值大的,比如PD - 1單抗,交易總額有望達到10億美元以上。從具體專案類別看,主要是兩種自研品種,一種是大靶點而且速度排在前面(市場表現好或者聯用潛力大的PD - 1類);另一種是比較新的靶點(SHP2、ROCK2等)和新型技術平台(像雙抗、ADC等)。
2021年初的時候,我們釋出了有關創新藥國際化的首篇深度文章,叫【中國創新藥企及管線「國際化」箭在弦上,整裝待發】。這篇文章以license - out作為核心話題,討論了中國藥企國際化的特色道路。2021年就是中國創新藥企全面開啟國際化行程的一年,年初好多家的PD - 1成功license out,到年中的時候維迪西妥單抗有了重磅交易,國內不少藥企透過相關的權益轉讓,開始在國際化道路上前行了。2022年被當作是國產創新藥在海外有收獲的一年。不過,年初因為信迪利單抗召開的ODAC會議,在一定程度上讓投資者對中國藥企國際化的信心受到了影響。但我們覺得這個ODAC會議有積極的地方,就是明確了中國自己研發的產品到海外做臨床研究和申報的主要途徑。傳奇生物的CAR - T療法西達基奧倫塞在海外獲批了,這表明FDA認可優質的差異化品種,也說明中國創新藥國際化的道路還是通的。所以,中國企業在研發的時候得重視差異化,不然同質化競爭會造成過度的內耗。

未來展望:新技術與平台效應
中國藥企迎來新技術帶來的新機遇。在藥物研發朝著差異化、國際化發展的浪潮裏,新興技術為藥企提供了展現自身特色、打造研發平台優勢的重要機會。中國在2010年之後才真正開啟創新藥研發的時代,傳統技術創新藥物的研發比海外晚了好幾十年。不過,中外創新藥企在新技術起步的時間點上幾乎相同,這就是新技術能讓國內藥企追趕上去,甚至在細分領域占據先發優勢的原因。現在,在抗體偶聯小分子藥物(ADC)、雙抗、細胞和基因治療、mRNA和Protac等方面,國內藥企已經有很多布局,在細分領域有了差異化的特色和優勢。
平台效應給中國藥企帶來更多機遇。綜合前面的討論,並非只有全新的靶點或者全新的適應癥才能成功,有差異化(像同一靶點不同適應癥、同一適應癥不同代際之類的)的研發也會有較好的獲批與商業化前景。對於產品性質本身差異化不大的競爭品種來說,平台價值非常關鍵,一個綜合性平台能讓臨床前研究、臨床研究以及CMC、註冊申報等流程更高效。對中國企業來講,國內招募患者的速度更快,患者數量更多,成本比美國等已開發國家低,所以國內的臨床試驗在推進速度上有自己的特點和優勢,也有希望在包含中國在內的國際多中心臨床中體現出速度優勢。拿百濟神州來說,它已經呈現出較強的國際化平台能力,據公司2021年年報,其有超過2200人組成的全球臨床開發團隊,並且在美國、歐洲和澳洲都有臨床團隊布局;公司正在執行90多項計劃中的或者正在進行的臨床試驗,累計招募了超過14500名受試者,其中大概一半是在中國以外招募的。恒瑞醫藥也組建了新的國際化團隊,引進臨床研發和市場方面的人才,公司的歐美CMO約瑟夫·艾德(Joseph Eid)以前是百時美施貴寶(BMS)的全球CMO;公司的研發創新升級了,在美國、歐洲、澳洲、日本都建立了專業的臨床研發團隊,全面啟動GPT(全球產品開發團隊)工作模式,建立海外智庫,更高效、高質素地完成全球臨床試驗。

3.3.2、在國內,BD已經變成傳統藥企創新轉型的關鍵策略了。
對於傳統藥企和創新藥企來說,選擇BD是一種雙贏。
BD(Business Development,也就是業務拓展)的意思是,透過像專利特許(License - in/License - out)、合作開發、股權投資、並購之類的方式來獲取創新技術或者產品,現在這已經是國內藥企常見的做法了。對於傳統藥企來說,因為全國集采的覆蓋範圍在慢慢變大,仿制藥的利潤一直在減少,所以傳統藥企急需轉型,這時候BD就成了傳統藥企補充產品種類、達成創新轉型的有用辦法;對於創新藥企來講,由於國家醫保談判變得常態化,藥能快點上市、進入醫保是創新藥能大量銷售的關鍵。要是沒有比較成熟的臨床或者商業化團隊的話,BD可以加快上市的速度、補上商業化方面的不足,而且能在產品開發比較早的時候就拿到現金收益,從而進一步提升創新藥企的周轉效率。
另外,BD合作對提高研發專案的成功率是有幫助的,能讓雙方共享資源,實作互利共贏。Nature Reviews Drug Discovery的一項研究表明,1997 - 2014年期間,合作專案成功的概率比非合作專案高得多。這就意味著研發合作能讓雙方發揮自身優勢,分擔研發時的風險,所以合作專案的成功率才會提高,對合作雙方而言這是個雙贏的選擇。
通常來講,臨床未滿足需求、和SOC的差異、市場獨占期或者專利技術,這些是決定BD價值的關鍵要素。另外,專案成功率、競爭狀況、銷售峰值潛力、所在的市場環境等,也都會對BD價值產生影響。拿專利特許協議來說,現在國內外常見的交易形式是「首付款+裏程碑付款+銷售額分成」。首付款是固定的數目,而裏程碑付款和銷售額分成是和專案進展相關聯的,要依據未來研發成功率和銷售峰值來確定。據LEK的研究表明,對於專利受讓方而言,因為前期新藥研發風險很高,首付款往往只占總交易價值的16%,研發和商業化裏程碑付款才是交易價值的主要部份,這樣就能確保交易雙方共同承擔後期的研發風險和收益。
跨國的大型藥企是全球醫藥BD交易活動裏的主要參與者。IQVIA的統計數據顯示,2021年全球醫藥BD數量排在前三位的藥企是默克、輝瑞和羅氏,其他那些交易頻繁的公司基本上也都是跨國大藥企以及部份CDMO企業。默克之所以活躍度很高,主要是和它的核心產品Keytruda(PD - 1單抗)有關系,在2021年,Keytruda和第三方腫瘤產品管線一共開展了35個臨床合作專案。另外,默克從Ridgeback引進了新冠口服藥molnupiravir,還就這種藥的仿制藥生產簽了一系列授權協定。

平均交易總額同比下降了,這或許表明市場熱度在降低。2021年,全球醫藥授權引進交易的數量比上一年增長了大概5%,達到了近五年的最高水平。不過呢,平均交易總額卻同比減少了8%,降到了4.52億美元。這可能是因為下半年美股Biotech市場的熱度降下來了,使得生物醫藥交易的估值也跟著下滑了。
在中國,生物醫藥BD的數量一年比一年多,傳統藥企對創新轉型的需求很強烈。
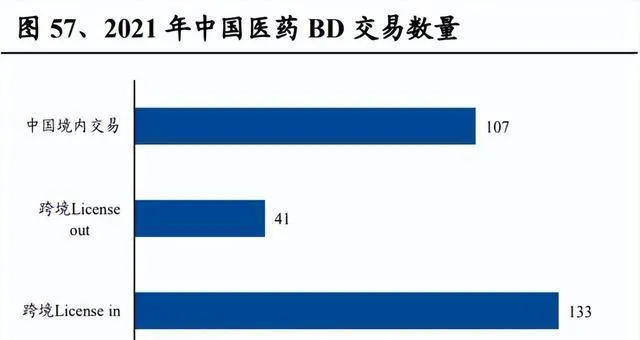
中國醫藥的BD(商務拓展)數量一年比一年多,主要是跨境License - in這種形式。美柏醫健統計過,2021年中國生物制藥這塊兒一共達成了281筆BD授權合作交易。這裏面呢,跨境License - in有133個,跨境License - out是41個,境內交易和聯合開發有107個。跨境BD的數量是逐年往上升的。
傳統藥企很需要創新轉型。像復星醫藥、信達生物、百濟神州、再鼎醫藥、恒瑞醫藥、華東醫藥、石藥集團、韓森制藥等企業就特別活躍,這裏面大部份是Big Pharma,還有些是有Biopharma潛力的Biotech公司,這就表明傳統藥企創新轉型的需求很強烈。
國內醫藥BD大多是靶點成熟或者已被驗證的腫瘤藥,可能是性價比更高的選擇。海外科學家回國創業熱起來後,國內就有了不少優秀的生物醫藥初創企業,國內傳統藥企和創新藥企之間聯合開發、轉讓權益也變得更頻繁了。從2021年國內十大BD交易情況看,交易專案基本上都是成熟或者已驗證的腫瘤靶點藥物,總金額比海外License - in低得多,對國內藥企來說可能是更劃算的選擇。(報告來源:未來智庫)
3.4、業務轉型並延展,原料藥在企穩發展的基礎上尋求新突破。
行業一直在擴大規模;環保政策的出台讓行業競爭格局得到最佳化;海外占比高,醫保控費的壓力就小。
Mordor Intelligence統計表明,2018年的時候,全球原料藥市場的規模是1657億美元。以後啊,不少重磅創新藥的專利會陸續到期,這樣的話,原料藥市場規模估計還會接著擴大呢。預計在接下來的幾年裏,全球對原料藥的需求會一直增長。等到2024年,市場規模有希望漲到2367億美元,年復合增長率會超過6.1%。
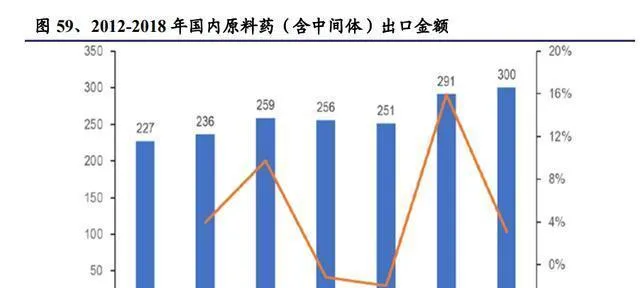
原料藥行業發展了好多年,現在競爭越來越激烈了。在中國,大多數原料藥企業已經從生產比較粗放的低端大宗原料藥,轉向生產精細的中高端特色原料藥了。這樣一來,企業深加工的能力越來越強,藥物的質素也跟著提高了。【水汙染防治行動計劃】之類的環保政策陸續出台以後,好多環保不達標、規模又小的中型和小型原料藥公司都關門大吉,永遠結束市場了。這些高汙染的中小企業結束後,行業競爭的格局變好了,行業的集中度提高了,剩下的原料藥公司盈利能力也有望提高。同時,國內生產原料藥的企業也在積極爭取國際認證,好讓中國的原料藥在海外賣得更多,認可度更高。中國現在是全球最大的原料藥出口國,正常年份能出口100萬噸左右,出口量大概占原料藥總產量的三分之一。中國醫藥保健品進出口商會統計的數據表明,2019年中國原料藥出口到亞洲、歐洲、北美洲等189個國家和地區,全年出口額達到336.83億美元。從2012年到2018年,中國化學原料藥出口交貨值從227億美元漲到了300億美元。近年來,醫保的覆蓋範圍一直在擴大,醫保資金的壓力也越來越大。跟其他主要靠國內收入的醫藥細分板塊相比,原料藥行業海外收入占比大,受到醫保控費的影響比較小。
原料藥企業大量涉足CDMO和制劑端,盈利水平明顯提升。
全球醫藥行業專業化分工的時候,醫藥CDMO行業的市場規模增長得特別快。Frost Sullivan統計過,2014年到2018年,全球醫藥CDMO行業的市場規模從178億美元漲到了268億美元,年均復合增長率是10.7%。這幾年,全球醫藥外包服務市場慢慢往新興市場轉移了。國際制藥企業想降低研發生產成本、提高經濟效益,國內醫藥行業的法規政策越來越完善,國內醫藥CDMO服務水平也明顯提高了,受這些因素影響,中國CDMO市場規模增長得更多了。同時,國內MAH制度全面施行,這給CMO/CDMO行業帶來了新的發展機會,對推動國內制藥行業的產業生態創新改革有很大意義。CDMO產業鏈和原料藥行業產業鏈特別像,原料藥企業在做原料藥業務時,化學合成方面積累了優勢,在拓展CDMO業務的時候就有天生的優勢。而且,原料藥企業和國際制藥企業合作的歷史很久,關系也很好,這也是原料藥企業CDMO業務能發展得很好的一個關鍵因素。
上遊化工品和海運價格都很高,這讓部份原料藥企業在短期內業績有壓力。以後仍然看好那些原料藥業務穩定,而且CDMO/制劑端發展迅速的原料藥企業。
今年,俄烏沖突和國內疫情散發等情況,讓中國化工產品價格指數(CCPI)、中國出口貨櫃運價指數(CCFI)還有上海出口貨櫃運價指數(SCFI)一直都處在高位。上遊化工產品和貨櫃運價高了,原料藥企業的成本就直接增加了,原材料企業的盈利能力也就受影響了,所以今年一季度好多原料藥企業利潤同比都下滑了。不過呢,大宗原料藥在過去幾年裏,有部份低端產能因為環保不達標之類的被淘汰了,競爭情況變好了,從年初到現在,大宗原料藥價格大多比去年同期漲了不少,相關企業大宗原料藥業務的盈利水平普遍有很大提高。另外,新冠藥潛在的用藥人群很多,短期內可能會有大量需求釋放,作為全球新冠藥物產業鏈的一部份,一些接到不少新冠藥訂單的原料藥企業在一季度的業績也很不錯。
3.5.1、醫療器材:硬科技助力國產替代,走向國際化成為一流。
這些年,咱們國家醫藥、機械、電子這些科技發展得特別快,國產的醫療器材已經漸漸突破好多技術上的難關了。往後十年,在中國醫療器材發展這事兒上,國產器材替代進口器材和產品走向海外是兩大主要方向。像測序儀、質譜儀、手術機器人這種大型的、高精尖的醫療器材已經開始替代進口產品了。與此同時,CT機、監護儀、體外診斷儀這些比較成熟的產品,全球化的行程也在加快,朝著全球一流的水平努力呢。這就是國產自己的技術創新和升級,不斷讓硬科技實力更紮實的一個過程。
大型醫療影像器材:慢慢攻克技術壁壘,國產品牌發展迅猛。
大型醫療影像器材有CT、MRI、PET這些細分產品,它們都是高精密儀器,是由上萬個零件構成的,還涉及到十幾萬項專利,在醫療器材行業裏,這是研發最難、技術壁壘最高的細分領域之一。中國的醫療影像器材行業總體起步晚,不過由於國家整體實力不斷增強、國民生活水平提高、人口老齡化、大力扶持醫療領域等因素的推動,中國醫療影像器材市場發展得特別快。好多年來,中國的大型醫療影像市場都被GE、飛利浦、西門子這些外資大企業壟斷著,國產品牌的市場占有率特別低,而且上遊的核心零部件(像CT球管、探測器、MRI超導磁體之類的)基本上全靠進口,外資企業以前差不多完全掌握著定價權,這就導致中國大型醫療影像器材的價格一直很高。最近20年,東軟醫療、萬東醫療、聯影醫療、明峰醫療等品牌發展起來了,醫療影像器材行業的國產化率一直在提高,像聯影醫療這樣的國產龍頭企業也漸漸有了和外資大企業競爭的實力。
另外,在比較高端的PET - CT這塊兒,像聯影這樣的國產企業表現也很出色。聯影醫療在2019年推出了一款超高端的PET - CT產品叫uEXPLORER(探索者),這可是全球第一台全景動態掃描PET - CT呢,掃描視野超大,能達到2米,靈敏度是傳統PET器材的40倍,全身掃描一次最快只要15秒就行。好多硬件效能參數都有突破,所以它能進行4D即時的全身動態代謝過程檢測,這就打破了傳統靜態代謝過程3D成像的限制。據經濟日報的數據,2016 - 2020年這五年,聯影醫療的PET - CT在國內新增市場占有率連續排名第一,在國內新增市場上已經成功超過了GPS這些外資大企業。
基因測序方面,國產測序儀正在奮力追趕,臨床套用也開始發展起來了。
測序是一種分子檢測技術,它的能力範圍非常廣闊。這裏說的「序」,就是多聚體生物大分子裏,組成單元形成的有方向的序列,像是蛋白質中的胺基酸序列、核酸中的核苷酸序列。序列對生命來說意義重大,它決定了人體細胞裏絕大多數構成分子的基本結構和功能。給體內的核酸、蛋白質這些生物大分子測序的話,能得到在臨床診斷上價值非常高的定性、定量資訊,從理論上講,這能涵蓋絕大多數人體生理過程。
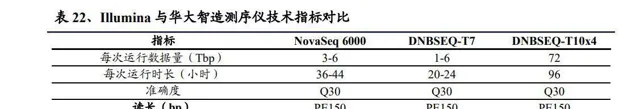
自從測序出現以來,「測」相關技術有了突破,這可是推動測序行業發展的重要力量。要知道,這些年中國的廠商在自主研發測序儀方面進步很大。這裏面有在NGS領域努力的華大智造、專門搞納米孔測序的齊碳科技,還有近期才進入這個領域的真脈生物、菲鵬生物等等。有些國產測序儀的效能在數據上已經趕上甚至超過了Illumina測序儀。就像華大智造的高通量測序儀DNBSEQ - T7,它每天的測序通量能達到6Tbp,比NovaSeq 6000每天3Tbp要高,而且測序成本方面還有一定優勢。DNBSEQ的核心技術是DNA納米球測序,這技術是華大智造收購Complete Genomics得來的。在這個基礎上,華大智造自己研發出雙色測序、CoolMPS、點陣芯片等關鍵技術。
手術機器人的底層技術要是能自主創新,很快就要進入高速發展階段了。
手術機器人被視作下一代外科手術的新形式,它的研發和制造涵蓋電子技術、機器人技術、精密機械、傳感器技術、訊號處理技術、生物化學、光學等好些學科,研發起來特別難。1999年達芬奇手術機器人在美國得到批準之後,就在全球手術機器人市場穩穩占據著龍頭老大的位置,在腔鏡手術機器人這塊兒都壟斷20多年了。最近幾年,國內陸陸續續有不少專門搞醫療手術機器人研發的國產企業冒出來,像微創醫療機器人、天智航、鍵嘉、術銳這些企業,在不同的外科手術領域都取得了一定成績。拿微創機器人來說,它正在研發的專案管線包含腔鏡手術、骨科手術、經自然腔道手術、泛血管手術、經皮穿刺手術這五大類手術機器人。
邁瑞醫療:國產替代產品大規模推廣,創新技術達國際一流水平。
邁瑞醫療的主要產品包含三大業務線,分別是生命資訊與支持、體外診斷還有醫學影像,其產品線在國內同行業裏是最全的,還能提供一站式整體解決方案。這三大業務線的產品都是醫院日常營運必備的基本器材。這些年,隨著技術發展、資本投入以及政策支持,國產替代的行程一直在推進。如今,國內差不多有11萬家醫療機構和99%以上的三甲醫院都在用邁瑞的產品。從2015年到現在,邁瑞推出了好多技術達到一流水平的高端產品,像BeneVisionN22、BeneFusion n系列、BC7500CPR、BS2800M等,這些產品在高端市場已經站穩了,而且正在加快向全球市場推廣。

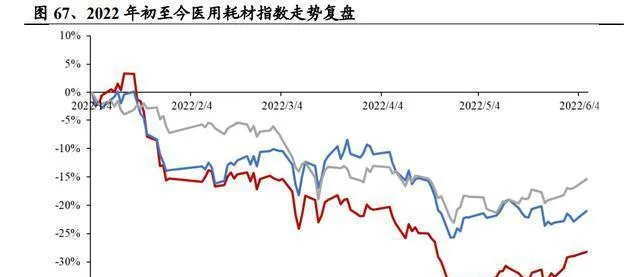
3.5.2、高值耗材:集采常態化發展,機遇和挑戰同在。
Eshare醫械匯估算,2019年中國高值醫用耗材的市場規模大概是1254億元,在醫療器械市場裏占比約20%。這些年它整體發展速度比較快,是醫療器械市場很重要的一部份。現在中國多數高值耗材細分領域還處在起步發展階段。從需求方面來說,創新產品的普及程度總體比較低,醫生和患者都還得長期不斷地接受普及教育;從供給方面看,多數領域還是進口企業占主導,國產企業在產品種類、效能、臨床認可度和研發創新能力這些方面都需要提高。能看到的是,目前主要高值耗材領域的國產化率整體比較低(除了心臟瓣膜這種國產企業先獲批推廣的領域),大部份產品國產化率不到50%,有些產品國產化率還不到20%。往後看十年,隨著基層需求不斷釋放、各種術式和產品不斷創新叠代、醫保覆蓋範圍擴大,我們預計中國高值耗材行業會保持較好的增長勢頭,國產替代依然是這個行業發展的主要方向。
我們覺得下面這幾類特點的公司或者賽道有希望嶄露頭角:1)賽道壁壘偏高、競爭形勢比較不錯:現在國內的耗材集中采購大多是臨床用量大、臨床使用成熟、市場競爭充分、同質化程度高的品種,競爭形勢好的賽道受到集采的壓力會比較小;2)商業化能力已經被證實:由於醫保控費對高值耗材的量價和競爭形勢都會有一定影響,並且產品持續研發創新需要投入大量資金,商業化能力被證實的企業自身造血能力比較好,在長期競爭裏有希望獲勝;3)跨賽道、平台型的公司:回顧美敦力、波科這些高值耗材大企業的發展歷程,不管是自己研發還是兼並收購,跨賽道布局基本上是所有大企業共同的選擇,平台化的好處一方面是能更好地發揮研發、渠道的協同作用,另一方面是能有效避免或者減輕集采這類醫保控費手段對公司經營的沖擊。(報告來源:未來智庫)
3.5.3、醫療器械合約研發生產組織(CDMO)
海外醫療器械產業鏈外包的比例在升高,醫療器械CDMO產業發展得很興旺。2010年美國【平價醫療法案】(Affordable Care Act)透過之後,支付方面變緊了,行業整合的壓力沿著醫療器械產業鏈從下往上傳遞,這就迫使產業鏈重新構建來提高效益。醫療器械企業(OEM)使勁兒往上遊找降低成本的辦法,使得醫療器械生產外包(CMO)很快從通用零部件發展到模組、整機;CMO也積極進行並購,想把垂直能力整合起來,在全球擴大產能。這些年,OEM和CMO的合作更深入了,醫療器械技術的整合度也提高了,這進一步催生了醫療器械研發、生產整體外包(CDMO)。全球醫療器械CDMO市場在2019年超過了500億美元,到2025年將會超過1000億美元,增速大概是10%,差不多是下遊醫療器械市場增速的2倍。
拿業務延展性當作標準,來預先判斷醫療器械上遊的「藥明」和「立訊」。和生命科學、消費電子、新能源車這些產業鏈上遊的企業比起來,醫械上遊企業有一些限制因素,像下遊細分種類繁雜、細分領域壁壘很高、客戶群的差別很大之類的,但也有比較優勢,比如技術和合規的門檻高、客戶的黏性很強等。在抓住從1到10的機會之後,業務延展性就會成為決定醫械上遊企業從10發展到100的重要因素。醫械上遊業務延展性的起點是1到10階段的切入之處,像客戶的質素、技術能力、下遊細分市場的容量等,而且會在跨行業、跨細分領域、自上而下拓展等路徑中實作,這其中的關鍵就在於企業的戰略決策能力、研發管理體系和投並購能力。

3.5.4、器械走向全球化
器械的全球化比藥品難多了。大家都知道,創新藥研發周期常常要10年。新藥研發出來上市後,還有大概8年的專利保護期。再看器械呢,它的產品「小叠代」更快,重點是要有更好的臨床效果,還要最佳化做手術的醫生的手術體驗。所以器械廠家得跟手術醫生有更緊密的聯系,靠「醫工結合」讓公司改進產品。這種更緊密的聯系會讓醫生對器械廠家的品牌更認可,客戶黏性也更強,藥品銷售在品牌黏性這方面好像就弱一些。這樣一來,器械走向全球化商業的路就比藥品更難走,前期得投入更多學術費用,花更長時間來讓醫生認可。
中國仍處於全球化的早期。當下,中國醫療器械企業整體規模都不大,在研發投入方面,和海外的醫療器械大公司比起來差得遠呢。2021年,國內營業收入排在前三的上市醫療器械公司,是邁瑞醫療(249.9億元)、英科醫療(162.0億元)和威高股份(131.8億元)。可它們跟全球醫療器械的巨頭企業比起來,差距還不小。全球醫療器械營業收入排前三的是美敦力(301.2億美元)、強生(229.5億美元)和雅培(225.9億美元)。再看研發費用,2021年國內研發費用投入最多的三家公司,分別是邁瑞醫療(25.2億元)、微創醫療(19.0億元)和樂普醫療(9.1億元)。全球醫療器械的龍頭企業美敦力,僅一年的研發費用就有27.5億美元(研發費用率為9.1%),這個數碼比國內好多頭部醫療器械公司的研發費用加起來還多得多。所以,國內的醫療器械要走向全球,還有很長的路要走。
【四、投資策略:把握醫藥產業升級下的新紅利】
醫藥行業的根本驅動力:全球產業鏈在「創新升級」狀況下的價值提升。
醫藥產業一直都以「創新升級」為主題。想要解除病痛的同情心,戰勝疾病的信心和決心,是促使醫藥健康產業不斷發展的動力,所以醫藥行業一直在發展。西方現代制藥業能夠興起和繁榮,是因為戰時和戰後有大量救治需求,而且在和平年代,醫療健康得到普及,人們追求高品質生活。探究醫藥產業發展背後的直接推動因素,也就是政策引導、人才眾多、技術革命、智能制造,它「從量變到質變」的特性決定了這個行業的內在發展路徑是周期性的。回顧近十多年中國醫藥行業的發展歷程,政策不斷發展推進,就像大浪淘沙一樣,每一批崛起的公司都有政策或者時代給予的內在發展動力。
中國醫藥產業在未來依舊會有「消費紅利」和「工程師紅利」。從2021年下半年起,醫藥業持續大幅調整,持倉達到了十年以來的最低水平。市場就不禁疑惑了,自費品種集采了,消費紅利還能不能持續呢?仿制創新藥價格不斷降低,創新紅利還能繼續嗎?國際環境發生變化了,工程師紅利還在不在呢?我們覺得答案是肯定的。首先是政策方面,政策的根本目的是推動生產力進一步提高,最佳化供給側,從而促使更高質素的創新和消費升級出現。其次是人才方面,70後的科學家在2010年左右大批回國,經過了十多年的發展,現在到了出成果的時候了,他們能適應政策的變化,並且有更強的發展能力。最後是技術方面,這是上世紀90年代興起的生命科學技術的傳播與融合,也是智能制造興起後產品競爭力的提高和飛躍。所以,中國醫藥產業未來的消費紅利、創新紅利、工程師紅利依然存在,而且會延伸到供應鏈高端制造和產業鏈國際化方面,催生出一批新的優秀企業。短期的調整只是在積攢力量,CXO、消費醫療、科技創新、國際化、上遊自主可控以及高端制造等領域在調整之後會再次發展起來。
(1)短中期:抓住疫情不確定時醫藥需求的韌性。
國內疫情現在被有效控制住了,全球第四波疫情也開始走下坡路了。不過,新冠病毒的突變方向還不確定,而且現在主流的Omicron毒株傳播得更快也更隱蔽,所以常態化的疫情防控可不能放松。生物醫藥有「剛需」的特點,在新冠疫情常態化防控的情況下,它的業績仍然有著不錯的韌性。回想2020年,頭部上市公司業績的恢復、供給端工業增加值、反映國內需求的社零數據、反映國外需求的工業出口交貨值,都在一定程度上展現了醫藥產業的剛性和韌性。
2020年新冠疫情在全球蔓延,全球對醫療防疫物資的需求一下子大增,可疫情防控期間產能降低了,運輸能力也下降了,所以各個國家越來越看重醫藥工業的戰略意義。現在全球醫藥的產業鏈和供應鏈都在加速重塑,咱們有可能碰上全球價值鏈(global value chain, GVC)地位提升的新機遇。和「原料 - 加工制造 - 服務」這種傳統模式比起來,近年來產業內部結構升級變得更重要了。就醫藥產業來說,因為它被監管得很嚴,所以拿到海外監管部門的資質認證、進入目標市場,並且充分知曉本土和目標市場的產業政策是非常重要的;而且這個產業對工藝、技術、產品等有很高的創新要求,這就使得本土創業和融資的環境、創新體系、產學研合作也成了提升產業綜合競爭力的關鍵因素;另外,在一些偏制造業的醫療器械領域,它的產業發展水平在某種程度上是由本土產業鏈的成熟程度決定的,像上遊裝備和核心元件的供應和發展水平就包括在內。

中國醫藥產業的國際化有利競爭一直在提升,從人口紅利發展到工程師紅利。在從勞動力密集型向技術、知識密集型轉變的時候,醫藥產業內部結構要最佳化升級,這就需要勞動者素質不斷提高。中國人口紅利逐漸向工程師紅利轉變,中國醫藥產業在國際上的有利競爭也很可能從單純的成本優勢,慢慢向差異化產品優勢、高效創新優勢(像創新藥領域在臨床研發方面的優勢,醫療器械領域醫工合作創新的優勢等)不斷提升,一些出口占比高的醫療器械企業,業務重心從OEM(原始器材制造商)轉向ODM(原始設計制造商),再轉向OBM(原始品牌制造商),這就是很好的例子。
(本文只是供參考,並不代表我們的任何投資建議。要是想要使用相關資訊,請檢視報告原文。)
精選報告來源:【未來智庫】。未來智庫 - 官方網站











