財聯社4月28日訊(編輯 金皓明) 4月26日晚,科創板公司百利天恒-U釋出2024年第一季度報告及2023年年報。公司在連續虧損3年後,在2024年第一季度一舉扭虧為盈,實作50.05億元凈利潤,同比去年同期增長3100%。公司表示,今年第一季度營業收入、凈利潤、總資產大幅增加,主要系收到百時美施貴寶(BMS)預付款所致。
此前百利天恒公告,2023年12月11日,公司全資子公司SystImmune與百時美施貴寶(簡稱「BMS」)就BL-B01D1(EGFR×HER3雙抗ADC)專案達成獨家特許與合作協定。該項合作協定由百利天恒全資子公司SystImmune與BMS達成,協定生效後,BMS將向SystImmune支付8億美元的首付款和最高5億美元的或有近期付款,在後續達成各項裏程碑後,SystImmune還將獲得最高71億美元的額外付款。
綜合來看,此次合作的潛在交易總額,最高可達84億美元。2024年2月8日,合作協定已正式生效。截至2024年3月7日,公司已收到由BMS支付的8億美元首付款(實際到賬金額須扣除銀行手續費),公司預計該款項將對2024年業績產生積極影響。
中國創新藥出海風頭正勁,開啟企業利潤空間
根據醫藥魔術方塊數據,2023年,國內共發生近70筆創新藥License-out交易,已披露交易總金額超350億美元,創歷史新高。據不完全統計,2023年下半年,就有百濟神州的替雷利珠單抗、君實生物的特瑞普利單抗、和黃醫藥的呋喹替尼、億一生物的艾貝格司亭α註射液等4款國產創新藥相繼在歐美上市。其中,替雷利珠單抗是中國首個在海外上市的生物藥,特瑞普利單抗是中國首個在美國上市的生物藥。2024年,國產創新藥出海的火熱勢頭仍在延續。機構數據顯示,2024年1月中國藥企的license out(對外特許)交易共計18筆,較2023年1月的5筆增長260%。
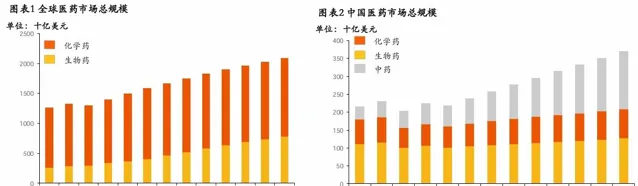
平安證券研報指出,全球醫藥市場2023年整體規模為1.585萬億美元,中國醫藥市場2023年的規模為2391億美元(以2023年人民幣兌美元年平均匯率約1:7.08換算),2023年全球醫藥市場總體規模為中國市場規模的六倍以上。預計2030年,全球醫藥市場規模可達到2.091萬億美元,中國的市場規模可達到3707億美元,全球醫藥市場規模仍為中國市場規模的五倍以上。出海可以讓國產創新藥找到更廣闊的市場,提升總銷售收入。
創新藥行業扶持政策頻出,行業發展「暖意融融」
今年3月「創新藥」首次寫入國務院政府工作報告之後,各地方政府對創新藥的具體支持政策正在漸次推出。
4月7日,北京市醫療保障局等9部門制定了【北京市支持創新醫藥高質素發展若幹措施(2024)(征求意見稿)】,要求加強對醫療機構的評價和激勵。4月7日,廣州開發區管委會、廣州市黃埔區政府釋出實施【廣州開發區(黃埔區)促進生物醫藥產業高質素發展辦法】,要求對創新藥、改良型新藥和生物類似藥,在國內臨床試驗研發費用投入1000萬元以上的,根據其臨床研發進度,分階段最高按實際投入臨床研發費用的40%給予資助:完成I、II、III期臨床試驗的,經認定,分別給予最高1000萬元、2000萬元、3000萬元扶持,單個企業每年最高資助億元。4月1日,【珠海市促進生物醫藥與健康產業高質素發展若幹措施(征求意見稿)】也對外釋出。檔提出,對創新藥研發期間獲得突破性療法和附條件批準的,再給予100萬元獎勵。鼓勵醫療機構牽頭或參與臨床試驗,縮短創新藥械研發周期。
產品銷售放量疊加出海,這些創新藥細分龍頭實作高增長

除去上述提到的今年一季度實作盈利超50億元的百利天恒-U外,多家創新藥細分賽道龍頭實作一季度凈利潤同比大幅增長。其中,艾力斯公告,公司核心產品甲磺酸伏美替尼片尼一線治療適應癥與二線治療適應癥順利續約納入國家醫保目錄,為公司 2024 年第一季度及至全年度的銷售業績奠定了良好基礎,對公司未來長期經營發展具有重要影響。公司今年第一季度實作凈利潤3.06億元,同比增長777.5%。受此訊息刺激,該股4月26日強勢報收漲停。早期產品開發方面,2024年3月,公司自主研發的具有全球知識產權的KRAS G12D選擇性抑制劑——註射用AST2169脂質體I期臨床研究獲得藥物臨床試驗批準。KRAS G12D突變是KRAS 突變的一種常見的亞型,存在於非小細胞肺癌、結直腸癌、胰臟癌等多種類別癌癥中。目前全球範圍內尚無KRAS G12D抑制劑獲批上市。
此外,國內老牌自免藥物龍頭三生國健在2024年第一季度實作凈利潤9111.91萬億,同比增171.88%。旗下三大主力藥品中:益賽普國內收入同比增長25.72%,賽普汀收入同比增長60.14%,健尼哌收入同比增長90.75%。而公司在研管線也取得積極進展:抗IL-17A 人源化單複制抗體(「608」):中重度斑塊狀銀屑病III 期臨床研究2023 年Q4 已達到主要終點和關鍵次要終點,III期臨床進行中。放射學陰性中軸型脊柱炎及強直性脊柱 炎專案均在II期受試者入組中。抗IL-5 人源化單複制抗體註射液(「610」):2023年Q4重度嗜酸性球哮喘患者的 臨床II期研究達到臨床主要終點,目前臨床III期啟動中。











