圖片來源:pixabay
一種已經停用的療法,可能導致艾爾茨海默病的「人傳人」。
撰文:黃雨佳 審校:clefable
幾十年前,數萬人註射了從屍體中提取的生長激素。這種療法曾風靡一時,而後因傳播疾病被叫停。科學家撥開層層迷霧,發現 艾爾茨海默病可能借由這種療法實作「人傳人」 。
屍體來源的生長激素
生長激素是由腦下垂體合成分泌的一種肽類激素,它能促進人體的發育和細胞增殖。如果人們在幼年時因遺傳、腫瘤等問題,導致腦下垂體功能異常,無法分泌足量生長激素,就可能身材矮小,患上「腦下垂體性侏儒癥」(又稱「 生長激素缺乏癥 」)。20世紀中葉,科學家已經發現了生長激素的作用,也曾嘗試從屠宰場動物屍體的腦下垂體中提取分離生長激素,用於治療生長激素缺乏癥。然而, 動物來源的生長激素似乎對人毫無效果 。無奈之下,研究人員只好轉向人的屍體。
1957年,美國塔夫茨大學(Tufts University)的科學家莫裏斯·拉本(Maurice Raben)成功從人腦下垂體中分離了生長激素。他收集了大量人類屍體的腦下垂體樣本,保存在丙酮中,然後用電動攪拌機將其打成勻漿,再真空幹燥成粉末。隨後經過萃取、沈澱、吸附等一系列步驟,他最終得到了生長激素成品。利用這種方法, 大約每1000個腦下垂體能幹燥出100克粉末,而從每100克腦下垂體粉末中又能提取出3~5克生長激素 。
拉本用於打碎腦下垂體的攪拌機(圖片來源:美國國家歷史博物館)
之後,拉本開始嘗試用這種人類屍體腦下垂體來源的生長激素(c-hGH)治療生長激素缺乏癥患者,一名17歲患者是他的第一個實驗物件。這位患者之前平均每年只能長高1.3厘米,但 經過10個月連續肌肉註射生長激素,他一共長高了5.3厘米,速度甚至略快於同等身高的普通孩子 。
這項實驗結果一經發表立刻引起轟動,生長激素缺乏癥患兒的父母紛紛希望孩子能參與此類治療。美國、英國、加拿大、法國等都建立了政府資助機構,專門收集屍體腦下垂體並分離純化c-hGH。 美國荷爾蒙與腦下垂體計劃(NHPP)每生產一批c-hGH,就需要來自16 000具屍體的腦下垂體 ,而患者一般需要每周多次註射c-hGH,平均治療時長更是長達4年。由於來源有限, c-hGH的供應十分吃緊,甚至一度實行配給制 。
然而,「好景」不長。截至1985年,美國食品和藥品管理局(FDA)已經收到至少3起接受c-hGH治療後出現快速進展且致命的神經退行性疾病的病例報告。 這些患者都曾在童年或青春期註射過c-hGH,並在治療後14~20年內出現了精神狀態惡化、語言和運動障礙、癡呆等癥狀。 最終,其中2名患者被診斷為克羅伊茨費爾特-雅各布病,即克雅氏病(CJD)。
克雅氏病是一種由於大腦中蛋白質錯誤折疊引起的罕見神經退行性疾病,美國和歐洲的發病率僅為每年每百萬人中一例。克雅氏病可以自發發生,但也可能因感染一類名為朊病毒的蛋白質,導致大腦中異常折疊的蛋白質積累、聚集、形成斑塊。通常,克雅氏病患者的年齡都超過50歲,而這些接受c-hGH後出現癥狀的人不過二三十歲。基於種種證據,美國疾病控制與預防中心(CDC)認為, c-hGH極有可能是傳播克雅氏病的媒介 。

生長激素缺乏癥患者註射生長激素後的各類生理指標變化(圖片來源:原論文)
因此,曾經火爆一時的c-hGH療法迅速被叫停。好在,隨著科技發展,美國基因泰克(Genentech)公司生產的第一代重組人類生長激素(商品名Protropin)那時已臨床試驗多年,美國FDA迅速批準了這款藥物,填補了市場空缺。利用c-hGH治療生長激素缺乏癥的方法正式成為歷史。據統計, 1959至1985年間,全世界共約3萬人註射了c-hGH ,其中英國至少1848例,美國超過1萬例。 截至2012年,全球大約450名患者因此患上克雅氏病。
系列問題浮出水面
故事並未隨著c-hGH的叫停而結束。由於朊病毒感染後的潛伏期較長,類似的病例一直在陸續出現。2015年,英國倫敦大學學院的約翰·柯林格(John Collinge)團隊在對8名因c-hGH患克雅氏病的逝者進行屍檢時, 除了在其大腦中發現導致克雅氏病的朊病毒外,還意外地在4名患者大腦的灰質和血管中發現了大量β-澱粉樣蛋白(Aβ)沈積 ,這同樣是錯誤折疊蛋白的聚集體。另外2名患者出現了局部Aβ病變,1名患者腦中也出現了少量Aβ,只有一例患者的Aβ檢測結果為完全陰性。
一般而言,大腦灰質中出現Aβ沈積是艾爾茨海默病的典型特征,而血管壁上的Aβ沈積是腦澱粉樣血管病(CAA)的指征,而CAA通常是艾爾茨海默病的先兆。此類疾病常見於老年人,但這些逝者的年齡範圍卻在36~51歲,因此研究人員懷疑他們可能攜帶某種與之相關的基因突變。但奇怪的是, 當研究人員檢測這些逝者的基因時,並沒能檢測到常見的與早發性艾爾茨海默病等神經退行性疾病相關的遺傳變異 。這些結果讓他們意識到,c-hGH不僅能成為傳播克雅氏病的媒介,還可能傳播了艾爾茨海默病。
可是,此前從未有過證據表明艾爾茨海默病能「人傳人」,於是研究團隊進行了更為深入的研究。他們首先想知道,這些患者註射的c-hGH批次中是否真的存在Aβ。因此,研究人員從英格蘭公共衛生局(PHE)那兒取得了8名患者當年接觸過的部份c-hGH樣品,它們已經在PHE密封儲存了30多年。結果, 所有樣品中均檢測出大量Aβ,同時也檢出大量tau蛋白 ,這是另一種科學家認為可能與艾爾茨海默病相關的蛋白質。
而且,樣品中Aβ的含量似乎與c-hGH的制備方法有關。在拉本等人成功從人屍體腦下垂體中提取出c-hGH後,經過研究人員的進一步最佳化,一系列c-hGH分離純化方法得以誕生,例如HWP和FL等方法。結果, 他們只在透過HWP制備的c-hGH樣品中檢測到了大量Aβ和tau蛋白,其他方法均未檢出 。同時,記錄顯示,所有這些大腦中出現Aβ沈積的患者,都曾註射過HWP制備的c-hGH。
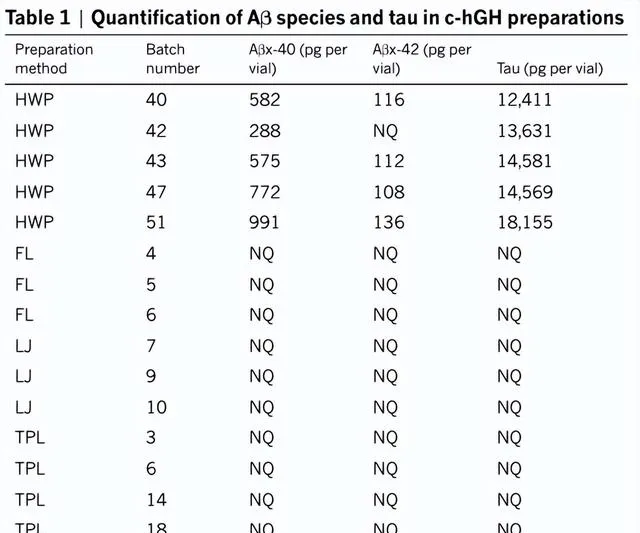
不同批次c-hGH樣品中的Aβ和tau蛋白含量(圖片來源:原論文)
接下來的問題是,這些樣品中的Aβ是否真的能誘發新的艾爾茨海默病。研究人員選取c-hGH樣品中的兩個批次註射進了基因編輯小鼠的大腦。結果, 接種這些樣品的小鼠腦內出現了大量Aβ沈積 。雖然與直接接種艾爾茨海默病患者的腦組織勻漿相比,接種c-hGH樣品的小鼠大腦中Aβ沈積程度較輕,但考慮到艾爾茨海默病患者大腦中的Aβ濃度比c-hGH樣品中高得多,這點並不奇怪。 只不過這些保存了數十年的樣品仍具有「傳染」活性,確實讓科學家萬分震驚。
不過,這些研究仍然只能說明c-hGH療法可能導致患者大腦出現Aβ相關的病變,可它真的能造成艾爾茨海默病嗎?後來,柯林格團隊又找到了另外8名接受過c-hGH治療的患者樣本。8名患者中的5名已經出現了早發性癡呆癥狀,1名有輕度認知障礙,1名出現主觀認知癥狀,剩下的1名患者並無癥狀。
利用影像學和生化手段,研究人員分析了他們的大腦,結果在不同患者體內發現了tau蛋白水平升高、Aβ沈積、腦萎縮等情況。 就連那位無癥狀的個體,大腦中也出現了部份和艾爾茨海默病相關的生物標誌物 ,例如纖維狀Aβ沈積和tau蛋白磷酸化水平升高。而與此前的研究物件相同,這些患者並未攜帶神經退行性疾病相關的遺傳突變。因此,研究人員認為,這些患者的癥狀和大腦改變是c-hGH療法帶來的,可以將其命名為「醫源性艾爾茨海默病」。
那麽,我們是否能就此得出結論,稱艾爾茨海默病具有傳染性呢?恐怕也很難,因為該研究的樣品數量太少,而c-hGH療法也已消失多年。不過,這項研究仍然給我們帶來了警示: 由於艾爾茨海默病患病率遠高於克雅氏病,因此需要考慮這種潛在傳播途徑對公共衛生的影響 。例如,重復使用的手術器械可能需要嚴格處理,避免透過這種方式傳播艾爾茨海默病的「種子」。
日常生活中我們並不需要擔心被傳染上艾爾茨海默病啦。
參考連結:
https://www.science.org/doi/10.1126/science.125.3253.883
https://www.sciencedirect.com/science/article/abs/pii/B9780433203407500052
https://academic.oup.com/jcem/article-lookup/doi/10.1210/jcem-18-8-901
https://www.cdc.gov/mmwr/preview/mmwrhtml/00000563.htm
https://www.newscientist.com/article/2414590-contaminated-hormone-injections-may-have-given-five-people-alzheimers/
https://en.wikipedia.org/wiki/Growth_hormone_therapy
https://www.ucl.ac.uk/news/2015/sep/possible-evidence-human-transmission-alzheimers-pathology
https://www.nature.com/articles/nature15369
https://www.nature.com/articles/s41586-018-0790-y
https://www.nature.com/articles/s41591-023-02729-2
本文來自微信公眾號「環球科學」。











