*仅供医学专业人士阅读参考


免疫治疗已经广泛应用于抗肿瘤治疗,但是它引起的严重免疫相关不良事件(irAE)也是阻碍治疗的一大问题。结肠炎是免疫治疗常见的irAE,尤其是在CTLA-4抑制剂治疗或其联合治疗中更为常见。
但是,相关的机制却没有在实验室中得到充分研究,因为小鼠很少在免疫治疗后出现肠道炎症。
本周,密歇根大学科学团队在【科学】杂志上发表论文,研究者们发现,
CTLA-4抑制剂诱导的结肠炎其实高度依赖肠道微生物
,
当研究者在实验室小鼠中定植野生捕获小鼠的肠道菌群,它们就能够表现出更接近人类的免疫特征,在免疫治疗后出现明显的结肠炎。
研究发现,肠道炎症是由产生IFN-γ的CD4 + T细胞过度激活,以及抗体Fc段诱导的调节T细胞(Treg)耗竭双重作用所致,缺乏Fc段的纳米抗体可以在保证抗肿瘤效果的情况下不引发结肠炎。

论文题图
由于在实验中,小鼠普遍表现出对免疫治疗导致的结肠炎的抗性,在研究相关问题时,需要额外使用干预措施诱导,例如使用葡聚糖硫酸钠(DSS)诱导或引入肠道炎症易感基因。
既往研究显示,免疫治疗效果与肠道维生物组成密不可分,因此研究者猜想,实验室中使用的小鼠一般饲养于无特定病原体(SPF)环境,这可能是它们免疫特征不同的原因。
研究者从野外捕获的小鼠中获得了参考肠菌(WildR),并尝试将其引入无菌小鼠(GF)建立免疫治疗诱导的结肠炎动物模型。实验结果可见, 接受CTLA-4和PD-1抑制剂治疗后,WildR小鼠出现了显著的肠道炎症,而定植了SPF小鼠肠菌的小鼠未见肠炎。

WildR小鼠在免疫治疗后可见显著肠炎
16s RNA测序显示,SPF和WildR肠菌α多样性和Shannon指数相似,但具体组成差异显著。
进一步实验发现,CTLA-4抑制剂和PD-1抑制剂联用与单独使用CTLA-4抑制剂都能诱发WildR小鼠肠炎,但是单独使用PD-1抑制剂不能诱发肠炎,这与人类研究中的表现是一致的。
研究者分析了CTLA-4治疗后的盲肠免疫细胞, 发现表达IFN-γ和IL-17的CD4 + 辅助T细胞(T H )的积累 ,提示免疫治疗相关结肠炎中显著的T H 1反应。
同时,研究者还观察到肠道中Foxp3 + 调节T细胞(Treg)的减少,尤其是其中RORγt + 外周诱导Treg(pTreg)亚群的选择性耗竭。 此前有研究发现, RORγt + pTreg具有明显的免疫抑制特征,如CTLA-4、IL-10、细菌反应性TCR的过表达 。
以上结果表明,CTLA-4抑制剂会导致肠道中的T H 1反应和RORγt + pTreg耗竭。
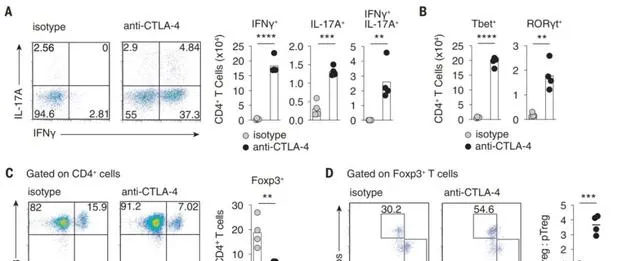
CTLA-4抑制剂会导致肠道中的T H 1反应和RORγt + pTreg耗竭
临床上,免疫治疗诱导的结肠炎经常与具有细胞毒性效应的组织驻留CD8 + T细胞有关,因此研究者也进行了相关的实验,但耗竭CD8 + T细胞并不影响结肠炎;使用IFN-γ中和抗体治疗小鼠则可显著减轻免疫治疗期间的肠道炎症。
可见,CTLA-4抑制剂导致的肠道炎症主要由CD4 + T细胞和IFN-γ驱动。
由于抗CTLA-4抗体通过Fc段介导的Treg消耗被认为是诱导肿瘤排斥反应的机制之一,研究者猜测这一现象可能也参与了免疫治疗相关结肠炎的发展。
在缺乏Fc受体的小鼠中,CTLA-4抑制剂果然并不会造成肠道炎症,也未观察到产生相关细胞因子的CD4 + T细胞,RORγt + pTreg耗竭显著改善。 由此可见Fc结构域对于CTLA-抑制剂诱导肠炎是必须的。
反过来想,不要Fc段,是否就能够一举解决这个副作用呢?
研究者选择了一种不含Fc段的CTLA-4单域抗体p1,并结合半衰期延长剂(HLE)。在MC38和CT26结肠癌小鼠中,p1-HLE都能表现出稳定的抗肿瘤效果,同时并不引发结肠炎。
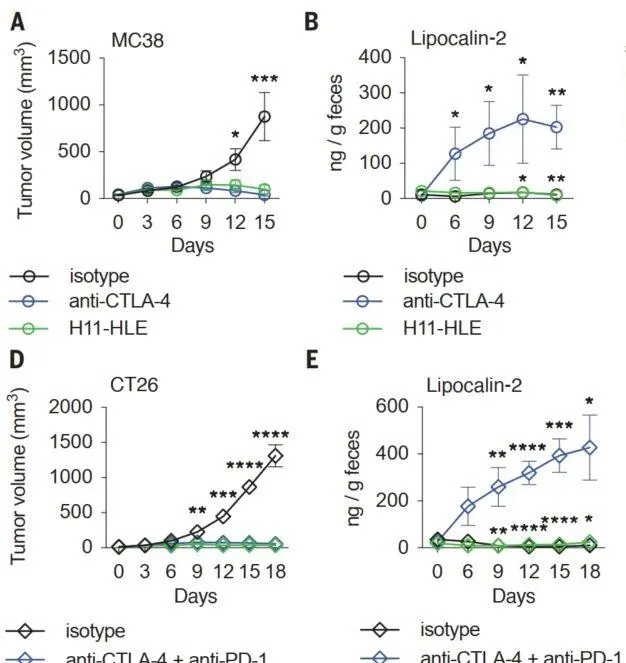
p1-HLE可表现出与抗CTLA-4抗体相当的抗肿瘤活性,同时不引发结肠炎
研究者猜测,自由生活的小鼠肠菌免疫原性更高,激活最佳抗肿瘤免疫反应所需的免疫耐受阈值可能更低,这是它们更容易在免疫治疗下发生肠道炎症的原因。
无论如何,找到了CTLA-4抑制剂致肠炎的关键,想必它还有更多的应用空间可以挖掘。
参考资料:
[1]https://www.science.org/doi/10.1126/science.adh8342

本文作者丨代丝雨











