來源:博藥公眾號
作者:頭孢

圖片來源:攝圖網
偶聯技術有多火?僅ADC(抗體偶聯藥物)領域,2017年之後就有超過10款新藥獲FDA批準上市,時至今日, 全球進入臨床階段的ADC藥物更是超過500余款 ,而萬物偶聯趨勢下,這個數碼還在無限擴大。
偶聯藥物有多卷?隨著DS-8201獲批上市,其突出的優勢為ADC藥物開發提出了更高的標準,也讓「差異化偶聯創新藥」成為主要趨勢,部份入局較晚的企業產品還在研就已喪失優勢,不得不思考「偶聯藥物未來又將如何發展」?
其實,與最初「魔術子彈概念」時代並沒有太大的變化,盡管蛋白質基因工程、化學偶聯等技術的持續進步,但偶聯藥物的發展方向仍主要圍繞新的靶抗原、新作用機制的有效載荷、新的抗體和載體形式等方面進行,而最大的不同就在於, 偶聯藥物方向更偏向於了靶向性 ,即更多具有特異定向作用的結構被用作了小分子毒素等有效載荷的載體。
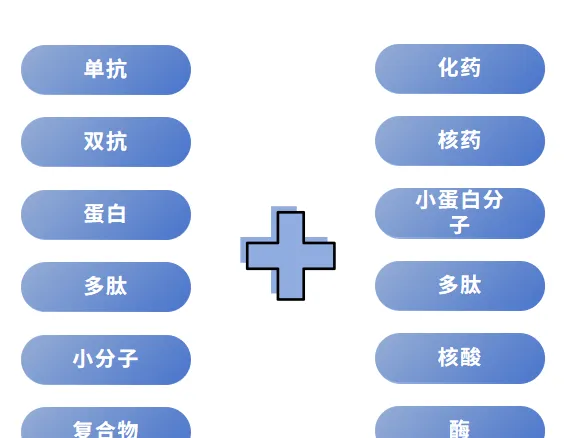
數據來源:公開數據整理
在此環境之下,組合用藥、精確遞藥的理念和套用場景進一步擴大,多種新興偶聯技術概念相繼湧現,業界也掀起了新興偶聯技術藥物研發熱潮。
差異化之路
非抗體蛋白偶聯的出現
原則上來講,偶聯藥物或許並不存在最優組合。
「萬物皆可偶聯」的核心理念之下,對最優組合的不斷探索反而促進了更多創新技術的出現,繼ADC爆火之後,PDC、FDC、SMDC、ISAC、RDC、ARC等多種技術如雨後春筍般不斷冒出。
多樣化策略之下,各種創新偶聯技術相較傳統ADC技術,或多或少都存在自身的核心優勢,如PDC較強腫瘤穿透性、更低的免疫原性與更低的生產成本;SMDC工藝簡單、安全性較好與安全性較高。而 除了抗體、多肽與小分子等常規的靶向分子,近來出現的「非抗體蛋白」也逐漸全新的研究領域。
非抗體蛋白偶聯藥物,即將靶向性蛋白分子與發揮藥效的效應分子(比如細胞毒分子,siRNA等)連線在一起,遞送效應分子到特定疾病部位發揮作用。其原理上與ADC的機理類似,最大區別就是靶向分子的不同,但相較前者卻有著核心的四大優勢:
免疫副作用更小: 蛋白偶聯藥物的蛋白部份大都來源於人類蛋白,例如重組人甲胎蛋白、重組人轉鐵蛋白等,相較於抗體、多肽能對人產生較小的免疫副作用。
靶點靈活: 對靶點的選擇相對靈活,很多企業在蛋白部份做了很多創新,例如Aro Biotherapeutics的Centyrins蛋白經過設計後可以與不同腫瘤抗原相結合。原則上可以避開偶聯藥物較集中的hear2等領域,去嘗試更新、更小眾的靶點方向。
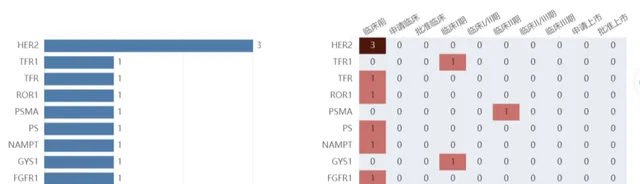
高效: 如外泌體偶聯藥物,可控的、模組化的藥物裝載與遞送,突破了抗體偶聯藥物(ADC)載藥率低、安全性有限的瓶頸,實作了更高效的提升效率。
穩定: 蛋白偶聯藥物的結構穩定性一般較高,且具有高效、可控的制藥載荷數量。
依從性高: 可以透過在蛋白中引入半胱胺酸來提高藥物的結合率,提高了藥物的依從性和便利性。
不過,由於蛋白偶聯技術總體上處於研究早期階段,某種程度上其優勢性與局限性都尚未研究透徹,後續或可能存在系列變化,但無論如何,從目前市面上相繼出現的非抗體蛋白偶聯技術來看,其臨床優勢也可初見端倪。
外泌體+轉鐵蛋白
蛋白偶聯的兩大典型技術路線
外泌體偶聯藥物(EDC)
2021年7月26日,Nature子刊Nature Biomedical Engineering線上刊發了中科院魏煒教授團隊聯合首都醫科大學陶勇教授團隊和昆士蘭大學余迪教授團隊共同署名文章,開發出外泌體偶聯VEGF單抗,利用Treg來源的外泌體(rEXS)為載體,透過基質金屬蛋白酶(MMP)敏感肽段(cL)連線VEGF抗體(aV),建立了rEXS-cL-aV體系。
後續透過外泌體化學偶聯技術,在外泌體上進行可控、可調節的多功能化改造,如構建融合表達特定蛋白和外泌體膜蛋白的質體,透過轉染等方式,讓該融合蛋白在外泌體來源細胞中大量表達,使得這些細胞分泌的外泌體能夠會攜目標融合蛋白。
圖片來源:參考資料1
最終,將外源性小分子化學藥物或生物大分子藥物與外泌體偶聯結合,形成外泌體偶聯藥物(EDC),實作高效、穩定、廣譜、可控的外泌體模組化藥物裝載與遞送,突破了抗體偶聯藥物(ADC)載藥率低、安全性有限的瓶頸。
在該領域上,天津外泌體科技有限公司是國內掌握該技術商業化的領先公司,根據其以往公布的數據顯示,其EDC藥物裝載率可達到92.3%、溶解性提高71.4倍、半衰期提高36.2倍、藥峰濃度提高3倍、 口服相對生物利用度提升2.6倍;裝載Herceptin抗體的外泌體呈現靶向效果相比對照組提升174.5倍,數據著實驚人。
至少就目前而言,EDC技術是外泌體領域最具商業化前景的技術,也是最為經典的非抗體蛋白偶聯技術。
重組人轉鐵蛋白偶聯藥物
鐵蛋白作為一種脫鐵蛋白組成的具有大分子結構的糖蛋白,通常情況下是由蛋白質外殼和鐵內核兩部份組成,在維持機體鐵代謝平衡和細胞抗氧化過程中起著關鍵作用,並且與炎癥、血管增生和腫瘤有關。
而人工條件下的鐵蛋白是具有空腔結構的籠形結構,外部的蛋白質外殼可透過基因和化學修飾增加靶向性,以達到提高遞送效率的目的,而空腔機構則可以用於裝載藥物,實作藥物的包載荷遞送。
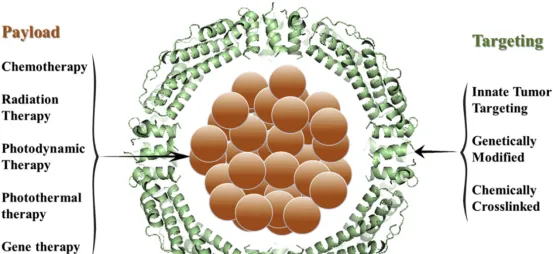
圖片來源:參考資料2
2005年鐵蛋白被成功用於包載遞送阿黴素,開啟藥物遞送領域新篇章,之後鐵蛋白藥物載體(FDC)的概念得以面世,相較ADC等常規偶聯藥物,其在安全性、滲透性、穩定性與靶向性等方面具有天然優勢,尤其是靶向性方面。
安全性: 鐵蛋白是來自生物體內的天然存在蛋白質,毒性低,具有良好的生物降解性和化石相容性,不容易引起排異反應。
滲透和滯留性 :由於鐵蛋白粒徑較小,使其易於逃脫網狀內皮系統的吞噬,半衰期較長,可在病變部位形成蓄積,增強藥效。
穩定性: 鐵蛋白的環境要求低,部份情況分解成亞基後仍能重組恢復籠狀結構,在制備和儲存工藝上要求簡便很多。
靶向性: 該領域鐵蛋白主要優勢主要有兩者,一者是 腫瘤靶向性 的基本要求,即腫瘤細胞對鐵離子的需求遠大於正常細胞,使得腫瘤細胞表面的轉鐵蛋白受體過度表達;二者是其 腦靶向性 ,由於鐵蛋白可跨越血腦屏障,同時轉鐵蛋白受體在血腦屏障中的表達水平明顯高於正常細胞組織,被寄希望於多種中樞神經疾病的藥物載體。
很明顯,就算同屬於蛋白偶聯藥物,在較EDC藥物高效、穩定與免疫副作用等相同的優勢,不同技術路線的蛋白偶聯藥物也有著差異化的優勢(如FDC的腦靶向性),而隨著生物醫藥基礎研究水平的上升,未來也有望誕生更多非抗體蛋白偶聯藥物,進一步豐富領域優勢性的同時,也可以拉高整個市場的天花板。
國內空白
蛋白偶聯藥物的藍海市場
就蛋白偶聯藥物市場而言 ,盡管近年來受ADC大火所帶動,但目前國內外對於該類別藥物的研究尚不完善,領域內多項技術仍處於臨床早期階段,相關性報道並不多。
據統計, 全球活躍蛋白偶聯類臨床藥物僅有20款 ,且絕大多數均處於臨床前階段,FutureChe的鑥[177Lu]Ludotadipep是目前臨床進度最快的管線產品。
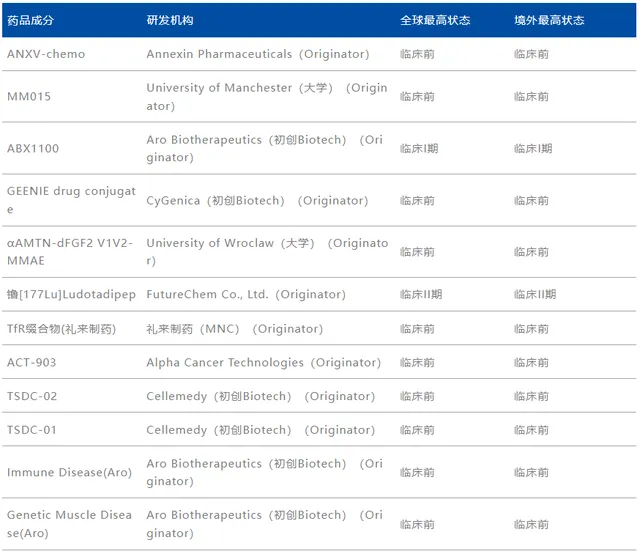
而就在研藥物適應癥來看 ,實體瘤、肺癌、乳癌等熱門疾病類別的集中度明顯更高,但同時部份蛋白偶聯藥物管線也選擇了自免、膿毒癥、代謝疾病與神經系統疾病為主要突破點。
其中,Aro Biotheraputics的 「ABX1100」 與Alpha Cancer Technologies的 「ACT-903」 是目前在研藥物中資訊披露較全面的品種,也是蛋白偶聯藥物中具有代表意義的品種。
「ABX1100」
ABX1100由ARO利用其Centyrins專利平台技術開發的核心產品,其特色的Centyrin蛋白FF0C具有優異的穩定性和溶解度、包括體積較小、可大腸桿菌生產,免疫原性較低,化學偶聯方法與生產方式相對比較簡單等優勢,特別適合靶向遞送寡核苷酸。
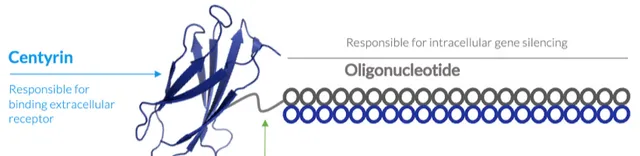
圖片來源:ARO官網
與抗體相比,Centyrins在早期內體中含量更高遞送速度更快,這可能Centyrins分子量小具有強滲透性優勢, 這樣更多的藥物分子能夠實作內涵體逃逸從而發揮其作用。
作為ARO針對龐貝病的一種全新潛在治療方法,ABX1100由結合CD71受體的Centyrin與特異性幹擾Gys1 mRNA表達的小幹擾RNA(siRNA)結合而成, 從而降低肌肉組織中Gys1酶的水平糊整體活性。 在GLP毒理學研究中顯示出良好的安全性,肌肉中Gys1 mRNA的持久減少,支持每月或每季度給藥的潛力,目前已獲得美國食品藥品監督管理局頒發的孤兒藥資格認定和兒科罕見病資格認定。
「ACT-903」
Alpha Cancer Technologies Inc. (ACT)是一家生物制藥公司,專註於其特有的重組人α胎蛋白(AFP)平台開發和商業化靶向免疫腫瘤學和免疫調節療法。

圖片來源:ACT官網
ACT-903作為ACT公司下一代ADC技術靶向α胎蛋白受體治療癌癥新方法的重要管線,其在2023 ASCO大會上首次亮相,是一種新型甲胎蛋白(AFP)-美坦胺酸偶聯物,在一項卵巢異種移植模型試驗中,ACT-903四種給藥方案下的臨床數據進行了對照,並觀察其細胞毒性,目前所有治療組體積縮小與生存期增加上均有明顯統計學意義。
ACT-903結合物對腫瘤體積的影響
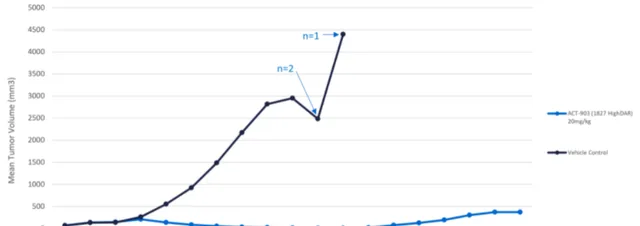
圖片來源:ACT官網
總研究結果顯示 ,ACT-903在卵巢異種移植模型中的安全性和有效性,以及在患者來源的癌癥類器官中觀察到的細胞毒性,支持ACT-903進入臨床研究。目前ACT已計劃在2024年送出ACT-903的研究新藥(IND)申請。
小結
隨著ADC藥物的越來越火、越來越卷,就連PDC、FDC、SMDC、ISAC、RDC等領域的競爭格局也同樣開始不容樂觀,稀有標的內容正在逐漸消失,如何在偶聯領域形成更差異化的競爭成為行業後續主要的思考方向。
但同時,藥物研發雖不能盲目跟風,但也不能為了差異化而差異化,應著重考慮臨床優勢與產業優勢,而對於蛋白偶聯藥物而言,盡管目前各項研究都尚處於早期階段,但其高效、穩定與特殊靶向性等特點也足夠吸引人。
或許,隨著未來研究的深入,蛋白偶聯藥物還真有望成為下一代更具潛力的ADC技術。
路漫漫其修遠兮,吾等仍將上下而求索。
參考資料:
-
外泌體的五大商業套用(三):外泌體偶聯藥物,精致顏容, 2024年01月14日
-
藥物遞送(八)——鐵蛋白技術, 藥物遞送,2021年10月08日
-
雙靶向Centyrin-siRNA偶聯物ABX300及其siRNA平台分析, 洞見conjugates 2022年06月19日
-
ALPHA CANCER TECHNOLOGIES PRESENTS NEW DATA FROM ACT-903, AN AFP-MAYTANSINE CONJUGATE, IN ONLINE PUBLICATION AT THE 2023 AMERICAN SOCIETY OF CLINICAL ONCOLOGY (ASCO) ANNUAL MEETING,ACT官網
博騰股份為全球藥企、生物科技公司、科研機構等提供從臨床前研究到藥品上市全生命周期所需的小分子藥物、多肽與寡核苷酸、生物大分子(mAb, ADC等)以及基因與細胞治療藥物等一站式服務解決方案,研發、生產、營運場地覆蓋中國(重慶、上海、四川、江蘇、江西、湖北)、美國、斯洛文尼亞、比利時、瑞士和丹麥等地。我們致力於以客戶為中心,為客戶提供卓越的全球化、端到端CDMO服務,讓好藥更早惠及大眾。
聲明:本文系藥智網轉載內容,圖片、文字版權歸原作者所有,轉載目的在於傳遞更多資訊,並不代表藥智網立場。如涉及作品內容、版權和其它問題,請在本平台留言,我們將在第一時間刪除。











