2024年剛開年,跨國藥企(MNC)加速掃貨中國創新藥。
1月2日,宜聯生物宣布已與羅氏達成全球合作和特許協議。雙方將合作開發靶向間質表皮轉化因子(c-MET)的下一代抗體偶聯藥物候選產品YL211。
1月5日,諾華宣布達成收購信瑞諾醫藥的協定,信瑞諾醫藥整體並入諾華中國。這也是諾華首次對中國生物技術公司發起的正式收購。

1月6日,拜耳、RTW投資公司宣布,分別以3500萬美元和1.27億美元對箕星藥業進行股權投資。箕星藥業是一家由RTW創立、現處於臨床階段的生物制藥公司。與此同時,拜耳集團處方藥事業部全球執行副總裁兼中國區總裁、拜耳集團大中華區總裁周曉蘭將加入箕星藥業董事會。

1月8日,強生宣布將以20億美元(約為143億元人民幣)的價格收購Ambrx Biopharma(安博生物),後者是一家臨床階段的生物制藥公司,擁有專有的合成生物技術平台,用於設計和開發下一代抗體偶聯藥物(ADC)。
在2023年末阿斯利康收購亙喜生物的訊息打響第一槍後,短短半個月,MNC就開始敞開購物車,大方「掃貨」中國Biotech資產。
2023年12月以來,就有羅氏4筆,BMS、阿斯利康3筆,諾華、艾伯維2筆,強生、GSK、禮來、BI等也都達成了新藥並購或者BD交易。而MNC「淘金」埠前移,以臨床前或Ⅰ期臨床階段切入早期研發創新生態圈。 值得一提的是,開年伊始這一波BD、並購「抄底」國內Biotech,國內本土大型制藥企業似乎頗為低調。
2024年,MNC能否繼續推高國內資產交易「天花板」?本土大型制藥企業是否將同樣掀起國內醫藥並購(M&A)浪潮?
01
「淘金」埠前移
MNC密集押註中國Biotech
MNC投資中國Biotech出現了新形式。
諾華收購的信瑞諾醫藥是一家專註於腎臟疾病及相關治療領域的臨床階段中國生物技術公司。其中,信瑞諾擁有2個針對免疫球蛋白A腎病(IgAN)創新藥專案在中國和新加坡的獨家權益:Atrasentan和Zigakibart,兩款產品均處於臨床研發階段。
Atrasentan為口服選擇性內皮素受體(ETA)拮抗劑,正在進行臨床III期開發。它在36周期中分析中展現出具有統計學意義和臨床意義的蛋白尿降低,成功達到了其3期研究的主要終點。另一款Zigakibart(BION-1301),皮下給藥的抗APRIL(一種促增殖誘導配體)單複制抗體,則已獲得中國藥品審評中心的批準,在2023年10月開始臨床III期研究。

羅氏對ADC領域首次出手的宜聯生物YL211專案,目前處於臨床申報階段。接下來,羅氏中國創新中心(CICoR)將與宜聯生物共同合作推動YL211專案進入臨床I期試驗階段,並交由羅氏負責後續全球範圍內進一步開發和商業化工作。羅氏將向宜聯生物支付首付款及近期裏程碑付款5000萬美元,另外還有近10億美元的開發、註冊和商業化潛在裏程碑付款,以及未來基於全球年度銷售凈額的梯度特許權使用費。結合2023年ADC出海交易,早期產品能夠短期變現5000萬美元,已相當不錯。
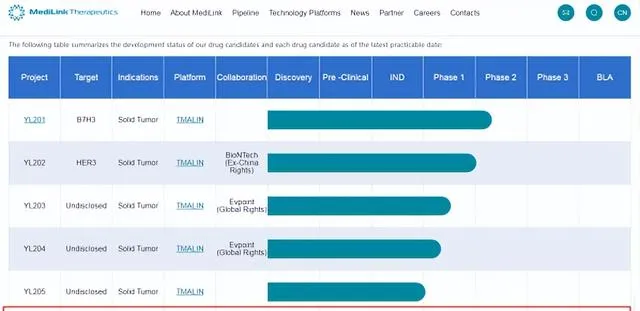
事實上,在2023年兩家biotech與阿斯利康合作的管線,也都是非常早期的階段。誠益生物ECC5004,尚處於1期臨床階段,僅有初步的數據讀出;誠益生物新藥ECC5004是一款口服小分子GLP-1藥物,目前正在美國進行針對健康受試者和2型糖尿病患者的I期臨床。而祐森健恒的UA022,甚至還只是一個臨床前的分子。
不管是誠益生物還是祐森健恒,都是規模極小的新生代biotech。今年6月份,誠益生物剛剛完成B輪融資;而祐森健恒更早,還只是一家僅完成了A輪融資的企業。
能夠挖掘到如此小規模公司的早期研發管線,足以說明如今MNC對國內市場、藥企的看重。這與過去的一些MNC在中國「淘金」思路有所不同。過去,國內這些早期管線,可能需要在國際頂尖會議上公布了相對驚艷的初步數據,才會引來大藥廠的合作意向。
在業內看來,早期專案相比於II/III期專案來說,臨床數據較少或仍處在臨床前階段,未來的風險更大,當然一定程度上也具備更大的潛力,但能否真正實作專案價值需要衡量。在早期階段合作對雙方來說其實都是風險與收益的平衡,借助合作方在後期開發上的能力來加快推進產品的快速上市,對雙方來說都可能是一種真正意義上的優勢互補,強強聯合。
02
早期專案合作
為何難覓國內大藥企身影?
回顧2023年,License out交易成為年度的重中之重。公開數據顯示,截至12月28日,2023年中國醫藥BD交易總額為505.9億美元,交易事件共124件。與2022年中國藥企BD交易數據相比,2023年交易總額增長147.3億美元,同比增長41%。License out事件數為53件,交易金額高達425.9億美元,占比84.2%。License in在中國醫藥交易中的占比開始降低,事件數僅為21件,交易金額為42.8億美元。

2023年國內創新藥License-out專案
(數據為【醫藥經濟報】新媒體中心整理,歡迎補充指正)
整體來看,中國創新藥企海外授權的最大特點就是:大部份是新成立的小公司。除了阿斯利康和羅氏,輝瑞和禮來也開始對國內創新藥早期專案和潛力技術平台青睞有加。
2023年3月,輝瑞旗下的公司Biohaven和高光制藥共同宣布,將高光制藥BHV-8000(也稱TLL-041)除中國地區以外的全球權利授予Biohaven。根據協定條款:Highlightll 將獲得 1000 萬美元的預付現金和1000萬美元股權投資,並有望獲得 9.5 億美元的開發和商業裏程碑付款,以及分級特許權使用費。該藥物預計於 2023 年進入Ⅰ期臨床。
禮來則是在今年5月份牽手AI制藥企業晶泰科技,簽署一項AI小分子新藥發現合作,針對某個未披露的創新靶點,由晶泰科技利用其特有的小分子藥物發現平台ID4Inno™研發首創新藥,填補未滿足的臨床用藥需求,預付款及裏程碑總收益可達2.5億美元。成立自2015年的晶泰科技,於2020年和2021年先後完成了3.19億美元C輪融資和4億美元D輪融資。
相比於跨國藥企對國內Biotech早期產品購買或股權和組織架構深入合作,本土大型制藥企業目前是以產品層面合作為主。 有業內人士指出,在收購層面,國內大藥企的全球市場競爭力依然較弱,尤其是創新藥如果只局限在國內市場的競爭,商業化價值難以充分挖掘,而一旦觸及海外市場,國內大藥企的全球化能力尚待進一步提升。
除此之外,在醫藥BD類交易進行過程中,雙方都會或多或少給予另一方有關醫藥研發產品的保密資訊、研發資料等。「過去一些國內藥企在BD誠信這方面做得不夠到位,容易出現‘套取商業資訊’的行為;另一方面,早期新藥研發面臨著非常大的資金及風險壓力,也讓國內藥企望而卻步。」上述業內人士如是指出。
值得關註的是,投資的回報與風險往往是並存的。
在一個又一個中國創新專案License out交易中,既有君實生物和Cohertus共同攜手將國產PD-1推向美國市場,皆大歡喜的成功案例;也有恒瑞與萬春醫藥核心產品因「出海」受阻深陷市場爭議,進而引發了交易糾紛……
事實上,引入臨床後期或已經在中國獲批的產品,對於MNC豐富產品管線而言充滿確定性;硬幣另一面,越是早期的專案,受到臨床開發速度、臨床療效數據、外部合作調整、市場環境變化等情況影響越大,這些都可能拉高BD交易風險。











