目前,人類對元素化合價的認知通常來自於對物質化學反應結果的總結,而不是從元素本身的構造和相互作用力機制上得來的。
本文所要闡述的是,每一種元素的化合價是從那裏來的,又是如何產生相互作用的問題。
我們知道,元素都有自己的化合價。化合價有同時帶上正價和負價的;有0價的;有正1價至正7價的;也有負1價至負7價的。並且某些元素的化合價還存在著一定的差異性,這應該是源於它們構成化合價的氘,所處元素的相位不同所帶來的同素異構體,這種情況應該多出現於第三及以上元素周期當中。
為了弄清楚化化合價的成因,我們必須先來了解一下微觀粒子間的電磁力作用規則。
1.質子只能與質子以串聯的方式形成氘和氚。因為,如果兩個質子極性相反的並聯,它們分別兩極間的間隔距離相對質子正負極之間的間隔距離要遠,導致結合力小於排斥力,因而兩個質子無法進行像氘與氘那樣的並列大串聯。
2.質子可以與氘相互結合。盡管質子的體長是氘體長的剛好一半,但它們之間是可以像兩個氘那樣結合在一起的。
3.氘可以與氘相互結合。兩個極性相反的氘,它們的兩極,分別借助於短磁力線進行異性連線,從而實作並列迴圈大串聯,這是原子核的形成和元素之間形成新化合物的電磁力作用中最普遍的方式。
4.氘可以與氚相互結合,但質子不可以與氚直接結合。
元素是從質子開始的。質子是一個帶有磁力線回路的磁場物;兩個質子可串聯成一個帶有磁力線回路的氘;三個質子可串聯成一個帶有磁力線回路的氚;氘與氘可結合成一系列化學元素。質子、特別是氚,可參與每一種元素形成它的系列同位素。
上述是元素構成的一些基本情況。
下面切入正題。化合價是元素之間成鍵的依托和前提條件,為了清晰說明化合價的成因。現借助於示意圖來一一加以說明:

圖為氫元素側檢視
一、氫元素
氫元素只有正一價。為什麽要賦予氫的化合價為正一價呢?因為氫的正一價意味著氫僅僅只有一個物質個體,它也只能被依附於另一個物體之上,才能形成新化合物。
氫元素,我們也可以把它形象地看成是一種陽性物質,陽性物只能與陰性物相匹配,氧就是一種典型的陰性物質。比如水分子,它是由一個氧原子和兩個氫原子組成。已知處於第二周期的氧元素,它在氦元素基礎上已經排入六個氘,離排滿八個氘還差兩個。這就是說氧元素中的氦核上面,還能接受帶陽性的兩個質子,或兩個氘、或同時接受一個質子和一個氘。正因為氧元素上面存在這兩個電洞位置,兩個氫才有機會與之相匹配,從而形成了水分子的。
圖為氦元素結構側檢視
二、氦元素
氦元素處於第一周期的末位,氦上面沒有凸出來多余的氘,所以不帶正價;又沒有凹進去的電洞,所以也不帶負價。氦元素自身狀態工整、左右對稱,核外磁力線飽滿,它對其它想加入的氫或氘的彈性排異力極大。故所以氫和其它帶正價元素上面的氘都無法與之結合。因此,氦元素的化合價只能是0價。
值得註意的是,假如強行往氦上面加一個氘,註意!是一個氘。這就意味著氦元素又開辟了一個新的周期。氦元素也就變成了鋰元素。
假如往氦上面強行加一個氫,氦就被強化成了一個氦的同位素了。即氦上面的一個氘上面再加上一個氫,這個氘就串聯成了一個氚,該同位素就由一個氘和一個氚結合成了氦五,而不是形成某種元素的化合價。
圖為鋰元素結構俯檢視
三、鋰元素
鋰元素是在氦元素基礎上加入一個氘形成的。
鋰元素處於第二周期中第一個加入進去的氘。這個氘十分顯眼的暴露在氦元素的外面,這凸出來的那個氘,就屬於正1價。
說到這裏,現在就可以下這樣一個關於化學價的定義了。即凡事已經排入原子核最外層的氘,有一個氘就是正一價;有兩個氘就成了正二價,有三個氘就成了正三價,有四個氘就成了正四價。
鋰元素除了擁有正一價以外,它應該同時還有-1價、-2價、-3價。甚至它還有-4價、-5價、-6價、和-7價的理由。因為鋰元素顯示,氦元素上面只排了一個氘,為了達到八個平衡,後面還有七個空缺的位置,這些空位從理論上講,它們應該能夠分別與其它多個帶有正價的元素進行化合的。當然,至於鋰元素除正一價外,是否還存在著其它幾個負價,還需要實驗證實,這只是透過理論推導所得出的預言。

圖為鈹元素結構俯檢視
四、鈹元素
鈹元素是在氦元素外加入兩個氘形成的。
依據凡是暴露在最外層的氘都是正價判斷。鈹元素擁有兩個正價。即正1價和正2價。 除此之外,鈹元素上面還存在六個空位沒有排滿。於是,理論上講鈹元素還同時擁有負1價、負2價、負3價、負4價、負5價和負6價。從理論上說,鈹不僅可以與一個或兩個帶有負價空位的原子結合,它還能與其它多個帶有正價的原子結合成不同的化合物。
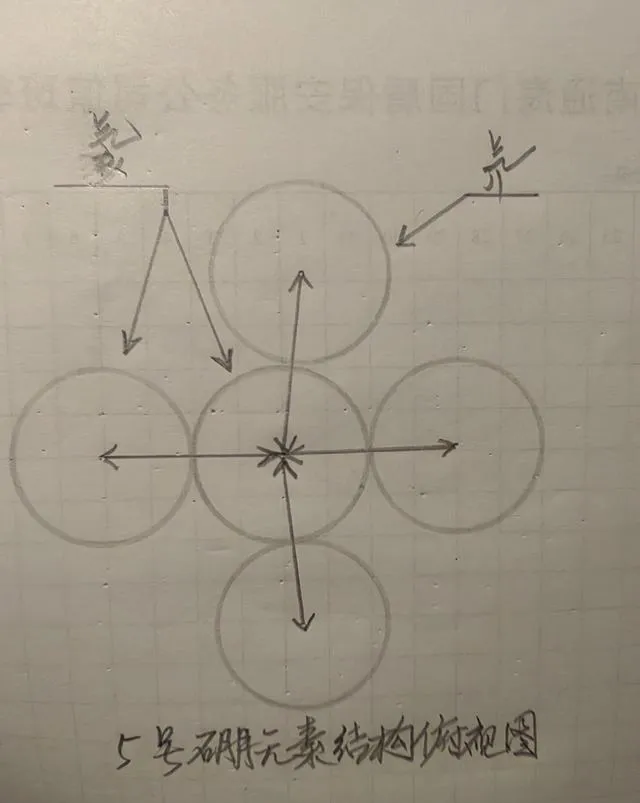
圖為硼元素結構俯檢視
五、硼元素
硼元素是在氦元素的基礎上,加上三個氘所組成。
硼元素上面的三個氘,分別為正1價、正2價和正3價。硼元素上面三個凸出來的氘,分別可與其它帶有三個負價的原子,包括不同的原子形成新的化合物。
硼元素除了三個正價外,它應該還存在著-1價、-2價、-3價、-4價和-5價。因為三個正價加五個負價,就等於氦元素上面總共擁有達到平衡狀態的八個價位。關於 硼元素的負價也屬於理論推匯出來的結論。
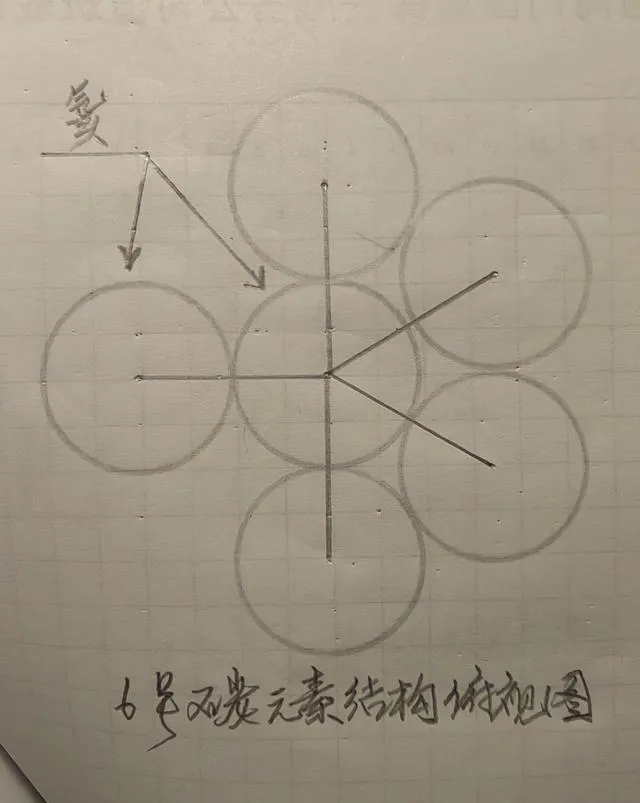
圖為碳元素結構俯檢視
六、碳元素
碳元素是在氦元素基礎上加4個氘形成。
由於這四個氘都暴露在元素的最外面,所以這四個氘都為陽性的正價。即+1價、+2價、+3價和+4價。但是碳元素上只排進去了四個氘,要是排滿8個穩定,那它還有四個空缺位置,這四個空位就是構成負價的空位:也就是-1價、-2價、-3價和-4價。所以碳元素擁有的四個正價,可與兩個帶有負2價的氧元素化合成二氧化碳,也可以與四個帶有正價的氫結合成甲烷。
碳元素同時擁有四個正價和四個負價,這是碳元素得以神通廣大的原因所在。

圖為氮元素結構俯檢視
七、氮元素
氮元素是在氦元素基礎上加上5個氘組成。
氮元素外層的5個氘都是正價。所以氮元素有+1價、+2價、+3價+4價和+5價。同時,氮在氦元素上面離排滿八個氘還有三個空位。所以氮元素同時還擁有-1價、-2價和-3價的三個負價電洞位置。
至此,我們已經知道,在化學反應中,負價一定是與正價進行陰陽匹配的。這也正好表明,元素間的作用力就是電磁力,並且是異性相吸力作用。同時也證明元素是由氘疊加而成的事實。
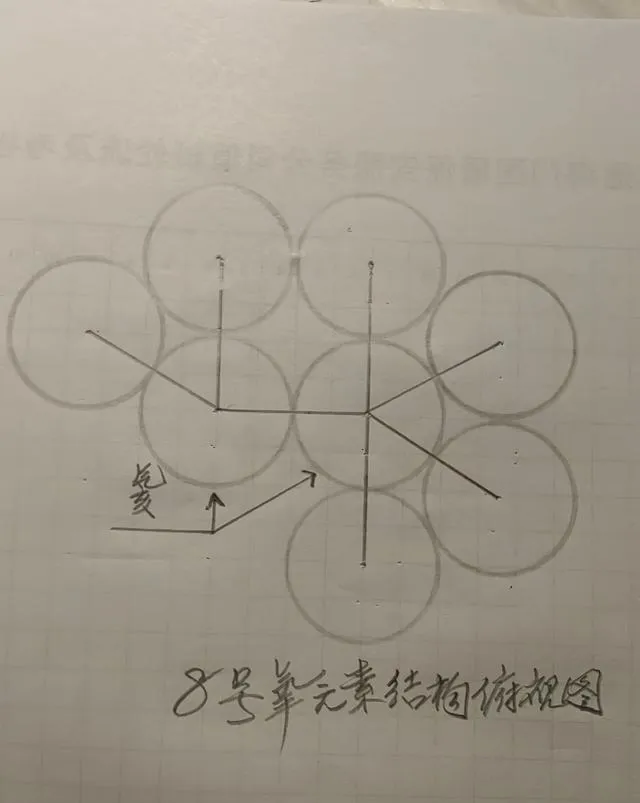
圖為氧元素結構俯檢視
八、氧元素
氧元素是在氦核的基礎上疊加上六個氘組成。
氧元素外層凸出來的六個氘,根據凸出為正,凹陷為負的判定。理論上氧元素可帶有六個正價和兩個負價。 但值得我們註意的是,由於氧元素外層已經排滿了六個氘,僅僅還剩下兩個空位沒排滿,所以氧的六個氘在空間結構上相互依靠、緊密有序,再加上它們的磁力線回路也比較豐滿,對外來某種帶有負價的元素賦有的彈性排斥力也比較大,因而其它帶有負價的原子想插入氧元素是相當困難的。尤其是氦上面的一個氘已經排滿了四個氘,排斥力非常大。而氦上面的另一個氘也已經排上了兩個氘,這兩個帶有正價的氘是有可能與其它帶有兩個負價的原子結合的。不過,結合時最好旁邊沒有帶正價的原子存在,否則帶兩個正價的原子就會先入為主地與氧上面的兩個負價相結合,從而沾滿了氧原子周圍的空間環境,導致氧上面兩個帶有正價的氘無法與其它帶有兩個負價的原子構成某種化合物了。
總的來說,氧原子通常顯負二價。
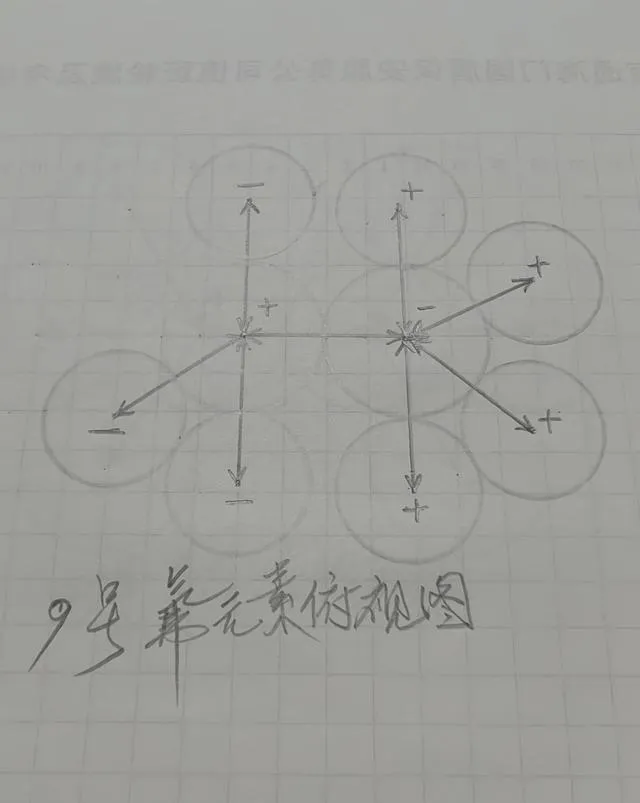
圖為氟元素結構俯檢視
九、氟元素
氟元素是在氦元素基礎上疊加上7個氘而成。
氟元素外層有七個氘,所以它們都是正價。氟元素還剩下一個空位沒有排滿。這個空位清晰地表明,它只有一個負價,因為它還有一個空位可用來與其它帶有正價的原子化合。比如可以接納帶有正價的一個氫,或者是其它帶有一個正價的原子形成某種化合物。
由於氟元素已經排進氦上面的氘多達七個。這就說明,理論上它可以擁有一至七個正價,但實際上它往往是利用不了的。其原因近似於上述已經描述過的氧元素,其情形的確有點尷尬。

圖為氖元素結構俯檢視
十、氖元素
氖元素是在氦元素基礎上再疊加上八個氘組成。
氖元素外層正好排滿八個氘。因此,它既沒有凸出來的一個氘,也沒有凹進去的一個空位。氖元素結構狀態平衡,磁力線豐滿有序,磁力線對外來原子的彈性排斥力十足。氖元素顯得十分自信、穩重和孤傲。所以它既沒有正價又沒有負價,它的化合價為0價。
關於元素上面化合價,暫時舉例說明於此。
綜上所述,元素的化合價有正價和負價之分。正價是元素最外層凸出來的那幾個氘,如鈹元素上面的兩個氘。
負價是元素最外層上沒有排滿氘的那幾個電洞,如氧元素上還有兩個沒有排滿的空缺位置。
元素形成化合價的口訣是:核外(元素最外層)之氘,「凸出為正,凹陷為負」。
當我們知道了元素化合價的來龍去脈以後,就能對著元素化合價圖譜,來做出相對明確的元素配伍,並進行遊刃有余的理論探究,以盡快找到形成某種新化合物的可能途徑。而不像是過去那樣,對著元素化合價的死板套用和實驗試錯。從而大大節約了化學研究的時間投入。











