你可知道?毒膠囊中主要有毒成分是什麽,今天我們要討論就是它-鎘。一種常見的對人體具有毒性的重金屬。毒膠囊中有毒的主要成分就是膠囊殼中含有超過20ppm(藥典)的鎘元素。人類對鎘元素的認識歷程可以追溯到1817年,當時德國化學家佛烈德利赫·斯特羅姆耐爾在分析一批氧化鋅時,意外地發現了鎘元素。他將這種新元素命名為「鎘」,因為它是從鋅礦石中分離出來的,與鋅相伴生。隨著時間的推移,人們逐漸認識到鎘對環境和人體健康的危害。例如,鎘汙染會導致土壤和水體受到汙染,影響農作物和野生生物的生長和生存。此外,長期接觸鎘也會對人體健康產生負面影響,如引發腎臟、肺部和骨骼等方面的疾病。另外鎘元素易在水稻,小麥中富集,是糧食中的重要監測專案之一。鎘渡層呈現很好的金屬光澤,在電鍍行業也套用很廣。下面我們來詳細介紹一下這個元素。

鎘元素的套用領域
鎘(Cd)是一種化學元素,其化學符號為Cd,原子序數為48。它是一種質地堅硬、有光澤的銀白色金屬,具有良好的延展性。以下是鎘元素在不同套用領域中的詳細介紹:
電池:鎘和鎘化合物在鎳鎘電池中廣泛套用。鎘作為一個陰極材料,在電池中發生反應,提供了高能量密度和長壽命的電源。
光學器件:鎘化合物在光學器件中起到重要作用。例如,鎘硒(CdSe)和鎘硫(CdS)等化合物可以用於制造光電二極管、激光器、太陽能電池等。
電子元件:鎘在電子元件中也有廣泛套用。例如,鎘鋅碲(CdZnTe)等化合物可用於制造半導體器件,如X射線探測器和核輻射探測器。
顏料:鎘化合物常被用作顏料,具有艷麗的顏色和良好的耐光性。其中最常見的就是鎘黃(CdS)和鎘紅(CdSe)。
防腐劑:鎘鍍層具有良好的耐腐蝕性,因此廣泛套用於金屬的防腐處理。
電子器件:鎘作為半導體材料,也被套用於太陽能電池、光電二極管等電子器件中。
合金:鎘可以與其他金屬形成合金,如鎘鍍層鋼和鎘鎘鉛合金。這些合金具有耐腐蝕性和高溫強度,被廣泛用於汽車制造、航空航天等領域。
需要註意的是,鎘是對環境和人體健康有害的物質。由於其毒性,對鎘的使用和處理需謹慎,要遵循相關的環境和安全規定。

鎘元素的物理性質
鎘(Cd)是一種化學元素,呈現銀白色,其物理性質如下:
相態:鎘在常溫常壓下為固態。它具有金屬特性,呈銀白色。
密度:鎘的密度較高,約為8.65克/立方厘米。這使得鎘具有一定的重量和質感。
熔點和沸點:鎘的熔點較低,約為321.1攝氏度(610.0華氏度),使其易於熔化和加工。而鎘的沸點較高,約為767攝氏度(1413華氏度)。
導電性:鎘是良好的導電體,具有較高的電導率。這使得鎘在電子器件中具有廣泛套用。
磁性:鎘具有鐵磁性,即在一定溫度範圍內會顯示出磁性。然而,當溫度超過特定臨界值(約為13.2攝氏度)時,鎘會變成順磁性。
膨脹系數:鎘的膨脹系數較大,即當溫度升高時,鎘的體積會擴大。這需要在設計和制造中考慮到其熱膨脹性質。
硬度:鎘的硬度較低,約為2.0摩氏硬度。因此,鎘較容易被加工和成型。

鎘元素的化學性質
鎘其化學性質如下:
反應性:鎘是一種活潑的金屬,與大多數非金屬元素發生反應。它可以與氧氣、硫、鹵素等元素反應,形成相應的化合物。
溶解性:鎘在酸性條件下溶解性較好,例如在鹽酸(HCl)或硝酸(HNO3)中能夠溶解。而在堿性條件下,鎘則不容易溶解。
氧化性:鎘具有兩個常見的氧化態,+2和+1。其中,+2氧化態是最常見的,稱為二價鎘。它可以透過與氧氣反應,形成二氧化鎘(CdO)等氧化物。
與非金屬元素反應:鎘與鹵素(氟、氯、溴、碘)反應可以形成相應的鹵化物,如氯化鎘(CdCl2)。鎘還可以與硫反應,形成硫化鎘(CdS)等化合物。
腐蝕性:鎘在濕氣和氧氣的存在下,會發生腐蝕。在空氣中,鎘表面會形成一層氧化鎘(CdO)的氧化膜,從而減緩進一步的腐蝕。
合金性:鎘可以與其他金屬形成合金,如與鉛形成合金(稱為錫鎘合金)。這種合金常用於電池、焊接和防腐等套用中。
需要註意的是,鎘是一種有毒金屬,其化合物對人體和環境具有危害。在使用和處理鎘及其化合物時,需要遵循相關的安全操作規定和環境保護要求,以最大限度地減少對健康和環境的危害。
鎘元素的生物特性
鎘(Cadmium)是一種重金屬元素,其在生物體內的生物特性引起了廣泛關註。以下是鎘元素的主要生物特性的詳細介紹:
1. 吸收: 鎘可以透過多種途徑進入生物體內,包括食物、水和空氣。在植物中,鎘透過根部吸收,然後在食物鏈中逐漸富集。
2. 分布: 一旦鎘進入生物體,它會在體內分布到各個組織和器官。鎘在肝臟、腎臟、骨骼和肺中的富集較為顯著。腎臟是鎘積累的主要器官,因為鎘主要透過腎臟排出體外。
3. 代謝: 鎘在體內的代謝相對緩慢,主要以兩價離子形式存在。在體內,鎘主要以金屬結合蛋白形式存在,其中金屬硫蛋白是一種主要的結合物。
4. 排泄: 鎘主要透過尿液排泄,尤其是透過腎臟。排泄速度相對較慢,導致鎘在體內的蓄積。
5. 對骨骼的影響: 鎘可以替代鈣進入骨骼,導致骨骼中的鈣被逐漸替代,從而影響骨骼的結構和穩定性。這可能導致骨質疏松和骨折的風險增加。
6. 對腎臟的影響: 鎘對腎臟有較大的毒性,尤其是對腎小管的損害。慢性暴露於鎘可能導致慢性腎臟疾病,並最終發展為腎功能衰竭。
7. 癌癥風險: 鎘被國際癌癥研究機構(IARC)評估為對人類可能致癌的物質。長期暴露於較高濃度的鎘可能與一些癌癥,特別是肺癌和前列腺癌,有關。
8. 對生殖系統的影響: 鎘可能對男性和女性生殖系統產生不良影響,包括降低生育能力和影響妊娠的結果。
9. 神經毒性: 鎘的神經毒性效應也受到關註,尤其是在長期或高劑量暴露情況下。
由於這些生物特性,尤其是其對腎臟和骨骼的毒性,人們對於避免過量攝入和暴露於鎘的關註日益增加。控制工業排放、合理用水、選擇低鎘含量的食品等措施都是減少鎘暴露的方法。
鎘元素的自然分布
鎘(Cd)在自然界中以極微量的形式存在,並且很少以純金屬的形式出現。以下是鎘在自然界中的分布情況:
地殼中含量:鎘是地殼中的一種稀有元素,其平均含量約為0.1毫克/千克。盡管在地殼中的含量較低,但它在一些礦石中存在,如鋅礦、銅礦和鉛礦中。
礦石中富集:鎘通常與其他金屬元素共生於礦石中。最常見的鎘礦石是鋅礦石中的鋅礬石(Sphalerite),其中可以含有可觀的鎘含量。此外,鎘還可以與鉛和銅礦石中的氧化物、硫化物和碳酸鹽等形成礦石。
水、土壤和植物中的存在:鎘可以透過天然過程進入水體和土壤中。它可以從巖石、礦石和土壤中被溶解或釋放出來,然後被吸附到土壤顆粒中。鎘也可以透過人類活動(如工業排放、農藥使用等)進入水體和土壤中。一旦進入土壤,鎘可以被植物吸收,並進入食物鏈中。

鎘元素的開采提取及冶煉
鎘的開采和冶煉提取主要有以下步驟:
礦石勘探:首先需要進行礦產資源勘探,尋找含有鎘的礦石礦床。常見的含鎘礦石主要是鋅礦石中的鋅礬石(Sphalerite),以及鉛、銅等礦石中的氧化物、硫化物和碳酸鹽。
采礦:確定了含有鎘的礦床後,進行采礦操作。具體采礦方法根據礦床類別和地質條件的不同而有所差異,例如露天開采、井下開采或水文挖掘等。
破碎和粉碎:采礦後,將礦石進行初步破碎和粉碎操作,以減小礦石顆粒的大小。
高溫冶煉:將礦石加熱到高溫,使其中的金屬部份熔化。透過冶金過程,將礦石中的金屬與其他雜質分離。在鋅礦冶煉過程中,鎘往往與鋅一起提取,並透過不同的分離和提煉技術將鎘分離出來。
電解:在一些冶煉工藝中,如電解過程,可使用電解池將金屬離子還原為純金屬。在這一步驟中,將使用電流和適當的電解質處理以提取純度較高的鎘。
精煉和提純:為了獲得高純度的鎘,可能需要進行進一步的精煉和提純步驟,例如真空蒸餾、氣相色譜等。

鎘元素的檢測方法
鎘元素的常用檢測方式主要包括原子吸收光譜法、原子熒光光譜法、原子發射光譜法、電感耦合等離子體質譜法和X射線熒光光譜法。下面對這些方法進行詳細介紹:
原子吸收光譜法(Atomic Absorption Spectroscopy,AAS):將樣品溶液吸入火焰或石墨爐中,透過電熱或化學反應使鎘原子蒸發、激發、吸收特定波長的可見光,透過比較吸收光強度與標準溶液的差別來測定鎘元素的含量。
原子熒光光譜法(Atomic Fluorescence Spectroscopy,AFS):將樣品溶液透過噴霧、電化學或熱解等方式產生鎘原子蒸氣,然後用激發光源激發鎘原子,鎘原子吸收能量後會發射特定波長的熒光,透過測量熒光強度來測定鎘元素的含量。

發射光譜法(Atomic Emission Spectroscopy,AES):將樣品溶液透過高頻電磁場,火焰或電弧等方式將鎘原子激發到高能階,在其回到基態時會發射特定波長的光線,透過測量這些光線的強度來測定鎘元素的含量。
電感耦合等離子體質譜法(Inductively Coupled Plasma Mass Spectrometry,ICP-MS):將樣品溶液透過等離子體噴霧進入質譜儀,利用高溫等離子體使樣品中的鎘原子與氣體離子化,然後透過質譜儀對離子進行分析和計數,從而確定鎘元素的含量。
X射線熒光光譜法(X-ray Fluorescence Spectroscopy,XRF):將樣品用高能X射線照射,樣品中的鎘原子受到X射線的激發後會發射出特定能量的熒光訊號,透過測量熒光訊號的強度來測定鎘元素的含量。
這些常用檢測方式具有靈敏度高、準確度高、選擇性好等特點,廣泛套用於環境監測、食品安全、生物醫學等領域中對鎘元素的檢測。不同的方法適用於不同樣品類別和含量範圍,選擇合適的檢測方法可以提高檢測效果
選擇合適的鎘元素檢測方法需根據具體樣品類別、測定要求和鎘的含量範圍等因素進行綜合考慮。

原子吸收法測量鎘元素的具體套用
在元素測量中,原子吸收法具有較高的準確性和靈敏度,為研究元素的化學性質、化合物組成以及含量提供了有效的手段。
接下來,我們使用原子吸收法來測量鎘元素的含量。具體的步驟如下:
制備待測樣品。將需要測量的樣品制備成溶液,一般需要使用混酸進行消解,以便於後續的測量。
選擇合適的原子吸收光譜儀。根據待測樣品的性質和需要測量的鎘元素含量範圍,選擇合適的原子吸收光譜儀。
調整原子吸收光譜儀的參數。根據待測元素和儀器型號,調整原子吸收光譜儀的參數,包括光源、原子化器、檢測器等。
測量鎘元素的吸光度。將待測樣品放入原子化器中,透過光源發射特定波長的光輻射,待測鎘元素會吸收這些光輻射,產生能階躍遷。透過檢測器測量鎘元素的吸光度。
計算鎘元素的含量。根據吸光度和標準曲線,計算出鎘元素的含量。
以下是一款儀器測量鎘元素用到的具體參數。

實際工作中需要根據現場具體需要和條件選擇適合的測量方法。以上這些方法在實驗室和工業中廣泛套用於元素的分析和檢測。
鎘(Cd)
標準物:純鎘片或鎘粒(99.99%)或優級純CdSO4·8pO。
方法:準確稱取1.000g鎘後,溶於少量(1+1)HNO3中,用水準確定容至1L,此溶液中Cd濃度為1000μg/mL。避光保存於聚乙烯瓶中。
火焰類別:空氣-乙炔,貧燃焰。
分析參數:
波長(nm) 228.8
光譜頻寬(nm) 0.4
濾波系數 0.3
推薦燈電流(mA) 2
負高壓(v) 317.50
燃燒頭高度(mm) 5
積分時間(S) 3
空氣壓力及流量(MPa,mL/min) 0.20
乙炔壓力及流量(MPa,mL/min) 0.05,1300
霧化器型號 WNA-1型吳氏金屬套玻璃高效霧化器
線性範圍(μg/mL) 0.01~1
線性相依系數 0.9994
特征濃度(μg/mL) 0.010
檢出限(μg/mL) 0.002
RSD(%) 0.55
計算方式 連續法
溶液酸度 0.5% HNO3
測量表格:
|
序號 |
測量物件 |
樣品編號 |
Abs |
濃度 |
SD |
RSD[%] |
|
1 |
標準樣品 |
Cd1 |
0.001 |
0.000 |
0.0003 |
42.5730 |
|
2 |
標準樣品 |
Cd2 |
0.050 |
0.100 |
0.0001 |
0.2803 |
|
3 |
標準樣品 |
Cd3 |
0.146 |
0.300 |
0.0010 |
0.7146 |
|
4 |
標準樣品 |
Cd4 |
0.230 |
0.500 |
0.0013 |
0.5552 |
|
5 |
標準樣品 |
Cd5 |
0.329 |
0.700 |
0.0007 |
0.2193 |
|
6 |
標準樣品 |
Cd6 |
0.448 |
1.000 |
0.0003 |
0.0724 |
校準曲線:
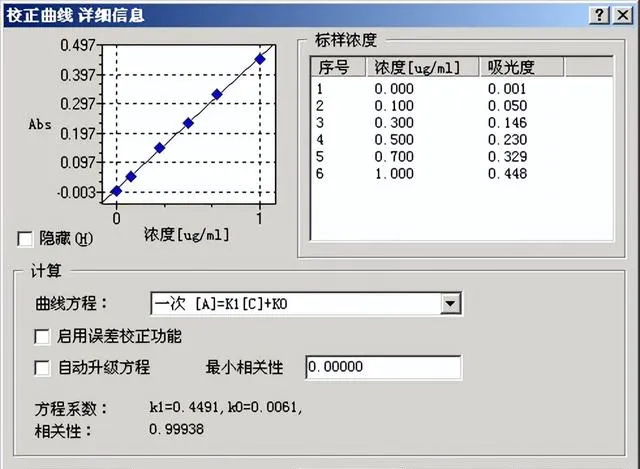
幹擾:
在空氣-乙炔火焰中未發現幹擾。燈電流嚴重影響靈敏度,低的電流有高的靈敏度。火焰狀態嚴重影響靈敏度,應仔細調節乙炔流量以獲得最大靈敏度。
實際工作中需要根據現場具體需要選擇適合的測量方法。這些方法在實驗室和工業中廣泛套用於鎘元素的分析和檢測。
鎘元素是一個具有重要套用價值的元素,但同時也對環境和人體健康存在潛在的危害。隨著科學技術的不斷發展和環保意識的提高,人們需要更加深入地了解鎘的性質和影響,采取有效的措施來限制其使用和排放,以保護弓境和人類健康。雖然鎘元素在現代社會中仍然發揮著重要的作用,但我們需要時刻警惕其潛在的危害,積極尋求更加環保和可持續的替代品,為未來的可持續發展做出貢獻。