
表观遗传学是指在不改变DNA序列的情况下对染色质进行修饰,它决定一个基因是否被表达,以及表达多少。组蛋白3上赖氨酸27的甲基化 (methylation of lysine 27 on histone 3,pK27me3),一种通常与基因抑制相关的修饰,在调节定向诱导分化(lineage commitment and differentiation)相关基因的表达中起作用。在许多癌症的发病机制中,这一关键标记体内平衡的改变已经成为一个反复出现的主题。pK27me的分布或水平波动可以由组蛋白本身的突变,或者其活性的变化而引起。pK27me突变的肿瘤患者有不良临床后果。目前针对异常pK27甲基化的治疗方法在临床中仍然被证明是有用的,了解受异常pK27甲基化影响的生物学后果和基因表达途径可能有助于确定新的治疗靶点和策略。
2022年,全球首款EZp/2双重抑制剂valemetostat获得日本监管部门批准上市,用于治疗复发/难治性(r/r)成人T细胞淋巴瘤(ATL)。 这是一款靶向表观遗传驱动因素的「first-in- class」抗癌疗法 ,尽管在临床上的实用性已获得证实,然而实际治疗中,其作用机制和肿瘤细胞的反应并不完全清楚。
日前,东京大学领衔的一支研究团队在顶尖学术期刊【自然】发表论文, 确定了抗癌药物valemetostat治疗成人ATL的疗效 ,并揭示了这类疗法如何针对 其靶点——pK27me3 (组蛋白p的27位赖氨酸三甲基化)重新激活抑癌基因的机制。这些发现对 以靶向pK27me3为代表的新一代表观遗传疗法 具有指导意义,有望为具有类似潜在病因的多种癌症带来新疗法。

pK27me3是染色体特定组蛋白上的一种甲基化修饰,即蛋白质上被添加上甲基(Cp)基团。这种修饰也被称为表观遗传,也就是在不改变DNA序列的情况下发生可遗传的基因功能变化。当基因及其启动子周围聚集甲基化组蛋白,其表达活性会受到重要影响,所以pK27me3具有抑制基因表达的作用, 过度pK27me3被看作癌症的主要表观遗传驱动因素之一 。
而EZp/2作为组蛋白甲基转移酶,受到EZp/2双重抑制剂的作用后,可以防止组蛋白p的甲基化。研究小组通过使用valemetostat治疗ATL患者的临床试验证明, valemetostat可以减少pK27me3,从而使癌细胞恢复多个抑癌基因的表达 。
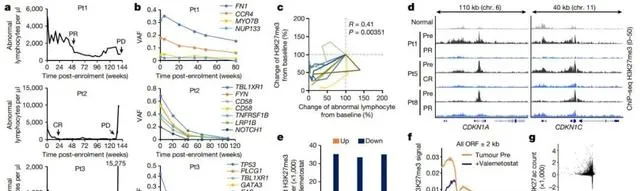
▲临床试验表明valemetostat的抗肿瘤作用(图片来源:参考资料[1])
论文作者介绍,ATL是一类具有多种基因突变的侵袭性瘤,在临床试验中, 患者接受valemetostat的治疗超过2年,肿瘤体积缩小,显示出持久的安全性和临床治疗反应 。
综合单细胞分析表明,EZp/2双重抑制剂可消除pK27me3形成的高度凝聚的染色质结构,恢复多个基因的表达,其中包括许多抑癌基因。
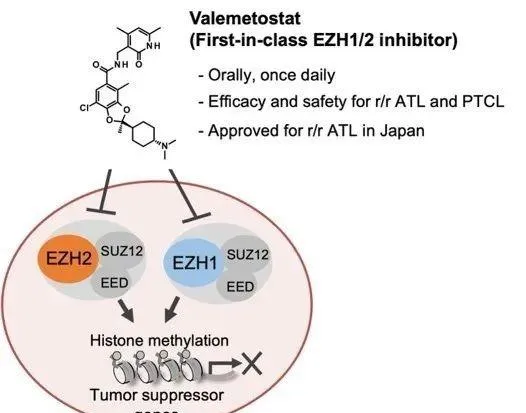
▲抗癌药物valemetostat的作用机制(图片来源:参考资料[2];Credit:Makoto Yamagishi/东京大学)
然而研究人员也注意到了 新的挑战 :如果患者长期接受治疗, 癌细胞可能会对pK27me3抑制剂疗法产生耐药性 ,从而导致癌症复发。在某些病例中,随着时间的推移,癌细胞出现了新的突变。尤其是同样可对pK27进行甲基化修饰的表观修饰酶PRC2复合物的获得性突变会导致pK27me3表达增加。
"EZp/2抑制剂是有效的治疗方法,但我们也发现了长期治疗导致耐药的机制,"研究论文的主要作者Makoto Yamagishi博士指出," 基于这种耐药机制,必须继续改进治疗方法,并开发出能提供更长期治疗效果的联合疗法 。"
参考资料:
[1] Makoto Yamagishi et al., (2024) Mechanisms of action and resistance in histone methylation-targeted therapy. Nature Doi: https://doi.org/10.1038/s41586-024-07103-x
[2] Researchers reveal mechanism of drug reactivating tumor suppressors. Retrieved Feb. 21, 2024 from https://www.eurekalert.org/news-releases/1034906











