引言
拉曼光譜是一種透過檢測分子的非彈性光散射,獲取其分子振動和轉動資訊的光譜技術。作為熒光或其它成像方式的補充,拉曼光譜成像具有「指紋圖譜」的高特異性、訊號不易光漂白、易實作多重成像等優點,成為分析化學、材料科學和生物醫學領域前景廣闊的成像技術。但是,每 1000 萬個入射光子中僅有 1 個會發生拉曼散射,因而小分子的自發拉曼成像訊號是極微弱、難以檢測的。為增強訊號,目前策略主要依賴於表面增強拉曼散射(SERS ) 技術,即透過在金、銀等基底材料表面吸附拉曼小分子,使訊號放大10 8 -10 11 倍,以實作高靈敏成像 【1,2】 。SERS技術自2006年用於活體成像以來獲得了顯著進展 【3,4】 。然而,這些SERS基底材料存在生物安全性問題,成為長久以來制約拉曼光譜成像技術在活體生物醫學套用及轉化的瓶頸問題 【5】 。
2024年8月21日,上海交通大學醫學院 肖澤宇 教授、復旦大學 陸偉 教授、中國科學院杭州醫學所 方曉紅 教授團隊合作,在 Nature Biotechnology 期刊線上發表了題為 「 Self-stacked small molecules for ultrasensitive, substrate-free Raman imaging in vivo 」 的研究論文, 揭示了一類特定結構的小分子,不需要依賴基底,僅透過自身的有序堆疊,實作在活體中的高靈敏拉曼成像,並提出一種新的拉曼散射增強機理-「堆疊誘導電荷轉移增強拉曼散射 ( SICTERS ) 」。 該研究為設計生物安全的高靈敏拉曼影像探針,並推進拉曼影像分析技術的活體生物醫學套用提供了新思路。

Nature Biotechnology 雜誌在同期以「 Small molecules self-organized in an orderly manner to enhance Raman signals 」為題,對該工作從領域問題、科學發現、未來方向等方面進行了詳細的亮點介紹,並配發了國際同行專家的評價,認為「 這個原創性的工作代表了活體拉曼生物成像技術的突破,並有潛力將其套用於臨床 - This original and innovative work represents a breakthrough for in vivo Raman bioimaging and its potential translation to clinical use. 」

在本工作中,研究團隊揭示一類以雙噻吩基取代作為供體 (D) 、苯並雙噻二唑作為受體 (A) 的共軛有機小分子 (如BBT) 。該類分子具有 D-A-D 的平面構象和平面內的多環振動模式;分子能夠在空間中有序自堆疊,使其相鄰分子間D和A單元的間距在3.6Å左右,促進了相鄰分子供體D和受體A單元間在分子內及分子間的電荷轉移。一個受體可以完全接收來自六個供體 (D2-A--D4) 的電子,其中包括兩個分子內供體和四個分子間供體。同時,一個供體可以向三個受體 (A-D--A2) 提供電子,包括一個分子內受體和兩個分子間受體 (圖1a) 。這樣的空間排列及交互作用重新調整了電荷分布,形成了新型的三維電荷轉移,顯著增加分子自身極化率,並增強拉曼散射。研究團隊將此類增強拉曼散射定義為堆疊誘導電荷轉移增強拉曼散射 (SICTERS) 。
為實作活體生物醫學套用,研究團隊進一步開發了SICTERS探針—臨床可用的DSPE-PEG劑型包覆的BBT奈米粒 (BBT NPs) ,該奈米劑型顯著提升了BBT在體內系統迴圈時的穩定性。此外,研究人員制備了與BBT NPs尺寸相近的SERS探針—金奈米粒 (Au NPs) ,並進行了拉曼散射增強能力的定量比較。研究表明,基於SICTERS技術的BBT NPs每個粒子的拉曼散射截面是基於SERS技術的Au NPs的1350倍。重要的是,基於SICTERS技術的BBT探針在組織臟器中的分布水平隨時間推移顯著降低,並經肝臟代謝糞便排出,血液學及組織學分析也展示了生物安全性;而SERS技術的金探針在肝臟等組織臟器中長期滯留,難代謝消除。
最後,研究團隊探索該技術用於活體術中微小腫瘤成像、無創淋巴回流成像及微小血管成像等生物醫學套用。結果表明,SICTERS探針能以最低1mg/kg的給藥劑量 (相比SERS探針4mg/kg) 實作術中對微小腫瘤的高分辨成像,並指導切除,降低術後復發及轉移。重要的是,SICTERS探針能夠活體無創的對淋巴回流及微小血管 (~11微米) 進行高分辨拉曼成像,這是SERS探針難以實作的 (圖1b) 。
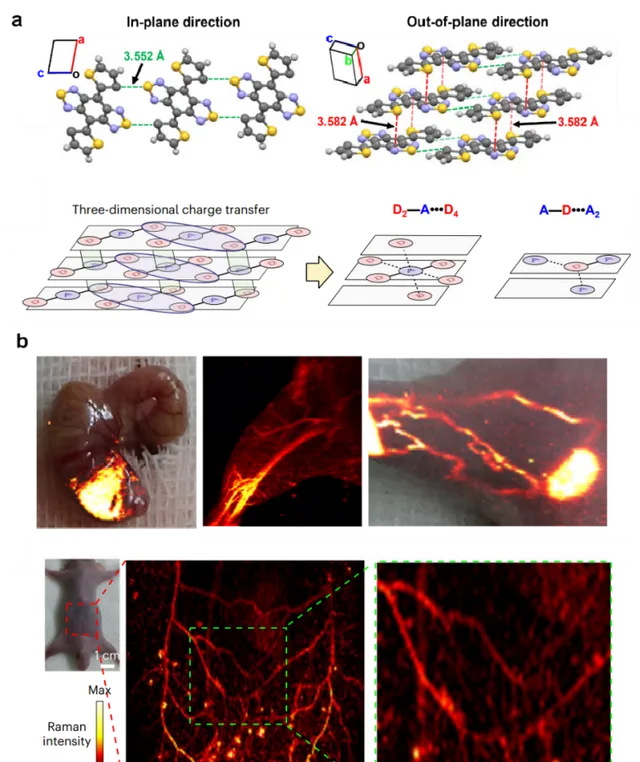
圖1:(a) 堆疊誘導電荷轉移增強拉曼散射(SICTERS)機理:具有D-A-D平面結構的小分子透過自身有序堆疊,促進了平面內和平面外的分子間電荷轉移。這種空間排列重新調整了電荷分布,實作了三維電荷轉移,從而大大增加了共振拉曼散射。 (b) SICTERS探針用於活體術中微小腫瘤成像、非侵襲性淋巴回流成像,非侵襲性腹部皮下微小血管成像。(Credit: Nature Biotechnology )
綜上, SICTERS在活體拉曼成像分析方面具有兩個顯著優勢:首先,SICTERS不依賴於基底增強,從而避免SERS可能帶來的生物安全性問題;其次,SICTERS技術在活體成像的靈敏度、空間分辨率和成像深度方面均優於SERS。SICTERS作為一種新的增強拉曼散射增強機理,為拉曼成像探針的分子設計提供了新的方向。
參考文獻
1.Fleischmann, M. et al. Spectra of pyridine at a silver electrode. Chem. Phys. Lett. 26, 163–166 (1974).
2.Langer, J. et al. Present and future of surface-enhanced Raman scattering. ACS Nano 14, 28–117 (2020).
3.Stuart, D. A. et al. In vivo glucose measurement by surface-enhanced Raman spectroscopy. Anal. Chem. 78, 7211–7215 (2006).
4.Qian, X. et al. In vivo tumor targeting and spectroscopic detection with surface-enhanced Raman nanoparticle tags. Nat. Biotechnol. 26, 83–90 (2008).
5.Dykman, L. & Khlebtsov, N. Gold nanoparticles in biomedical applications: recent advances and perspectives. Chem. Soc. Rev. 41, 2256–2282 (2012).
https://www.nature.com/articles/s41587-024-02342-9
責編 |探索君
排版|探索君
文章來源|「BioArt」
End











