
表觀遺傳學是指在不改變DNA序列的情況下對染色質進行修飾,它決定一個基因是否被表達,以及表達多少。組織蛋白3上賴胺酸27的甲基化 (methylation of lysine 27 on histone 3,pK27me3),一種通常與基因抑制相關的修飾,在調節定向誘導分化(lineage commitment and differentiation)相關基因的表達中起作用。在許多癌癥的發病機制中,這一關鍵標記體內平衡的改變已經成為一個反復出現的主題。pK27me的分布或水平波動可以由組織蛋白本身的突變,或者其活性的變化而引起。pK27me突變的腫瘤患者有不良臨床後果。目前針對異常pK27甲基化的治療方法在臨床中仍然被證明是有用的,了解受異常pK27甲基化影響的生物學後果和基因表現途徑可能有助於確定新的治療靶點和策略。
2022年,全球首款EZp/2雙重抑制劑valemetostat獲得日本監管部門批準上市,用於治療復發/難治性(r/r)成人T細胞淋巴瘤(ATL)。 這是一款靶向表觀遺傳驅動因素的「first-in- class」抗癌療法 ,盡管在臨床上的實用性已獲得證實,然而實際治療中,其作用機制和腫瘤細胞的反應並不完全清楚。
日前,東京大學領銜的一支研究團隊在頂尖學術期刊【自然】發表論文, 確定了抗癌藥物valemetostat治療成人ATL的療效 ,並揭示了這類療法如何針對 其靶點——pK27me3 (組織蛋白p的27位賴胺酸三甲基化)重新啟用抑癌基因的機制。這些發現對 以靶向pK27me3為代表的新一代表觀遺傳療法 具有指導意義,有望為具有類似潛在病因的多種癌癥帶來新療法。

pK27me3是染色體特定組織蛋白上的一種甲基化修飾,即蛋白質上被添加上甲基(Cp)基團。這種修飾也被稱為表觀遺傳,也就是在不改變DNA序列的情況下發生可遺傳的基因功能變化。當基因及其啟動子周圍聚集甲基化組織蛋白,其表達活性會受到重要影響,所以pK27me3具有抑制基因表現的作用, 過度pK27me3被看作癌癥的主要表觀遺傳驅動因素之一 。
而EZp/2作為組織蛋白甲基轉移酶,受到EZp/2雙重抑制劑的作用後,可以防止組織蛋白p的甲基化。研究小組透過使用valemetostat治療ATL患者的臨床試驗證明, valemetostat可以減少pK27me3,從而使癌細胞恢復多個抑癌基因的表達 。
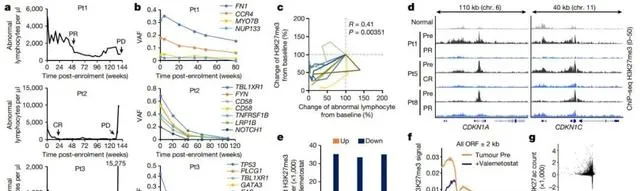
▲臨床試驗表明valemetostat的抗腫瘤作用(圖片來源:參考資料[1])
論文作者介紹,ATL是一類具有多種基因突變的侵襲性瘤,在臨床試驗中, 患者接受valemetostat的治療超過2年,腫瘤體積縮小,顯示出持久的安全性和臨床治療反應 。
綜合單細胞分析表明,EZp/2雙重抑制劑可消除pK27me3形成的高度凝聚的染色質結構,恢復多個基因的表達,其中包括許多抑癌基因。
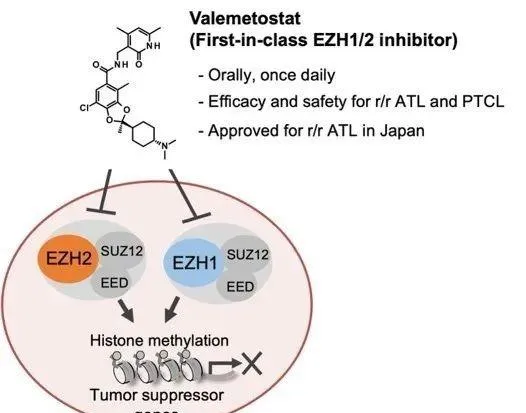
▲抗癌藥物valemetostat的作用機制(圖片來源:參考資料[2];Credit:Makoto Yamagishi/東京大學)
然而研究人員也註意到了 新的挑戰 :如果患者長期接受治療, 癌細胞可能會對pK27me3抑制劑療法產生耐藥性 ,從而導致癌癥復發。在某些病例中,隨著時間的推移,癌細胞出現了新的突變。尤其是同樣可對pK27進行甲基化修飾的表觀修飾酶PRC2復合物的獲得性突變會導致pK27me3表達增加。
"EZp/2抑制劑是有效的治療方法,但我們也發現了長期治療導致耐藥的機制,"研究論文的主要作者Makoto Yamagishi博士指出," 基於這種耐藥機制,必須繼續改進治療方法,並開發出能提供更長期治療效果的聯合療法 。"
參考資料:
[1] Makoto Yamagishi et al., (2024) Mechanisms of action and resistance in histone methylation-targeted therapy. Nature Doi: https://doi.org/10.1038/s41586-024-07103-x
[2] Researchers reveal mechanism of drug reactivating tumor suppressors. Retrieved Feb. 21, 2024 from https://www.eurekalert.org/news-releases/1034906











