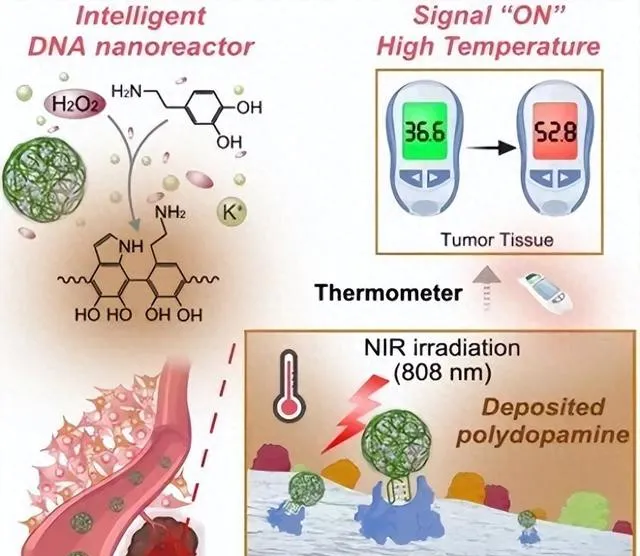
近日,上海交通大學研究員楊宇和團隊構建出一種智能 DNA 納米反應器(iDNR,An intelligent DNA nanoreactor),其遵循「AND」布爾邏輯演算法。
(來源:Angewandte Chemie International Edition)
iDNR,是一種智能型核酸生物材料。多價 AS1411 核酸適體和血紅素,是它的兩大組成成分。
iDNR 主要擁有兩大功能:第一,它能夠特異性結合腫瘤標誌物核仁素;第二,它具有響應腫瘤微環境過氧化氫的酶促催化活性。
在這兩種功能共同作用之下,可以構成一種「AND」邏輯門, 這種邏輯門擁有多個影響參數。從而能夠以智能化的方式實作對多巴胺受質的催化,產生光熱物質聚多巴胺,並在腫瘤部位實作有選擇性的沈積。
在這種設計方案的加持之下,iDNR 能夠透過易被讀取的方式,實作腫瘤的在體成像。
相比流式細胞術和光聲成像這兩種傳統技術,iDNR 所表現出的效能完全不遜於以上兩者。更重要的是,在使用 iDNR 的時候根本不需要昂貴的儀器。
此外,由於 iDNR 對於腫瘤組織具有高度的選擇性,因此可被用於實作精準的腫瘤光熱治療,即透過對腫瘤組織進行智能加熱,從而達到殺滅腫瘤的作用。
同時,iDNR 還可以介導腫瘤光熱治療,如果再和免疫檢查點阻斷治療方法加以結合,就能讓遠端腫瘤的生長得到進一步的抑制,增強免疫系統對於腫瘤的作用。
總之,由於「AND」布爾邏輯演算法具備多參數響應的能力,因此由其介導的 iDNR 策略,可以讓基於光熱的易讀腫瘤成像效果得到改善,從而實作更精準的腫瘤治療。
在具體的套用上,作為一款新型腫瘤成像方法,iDNR 除能實作簡單和易於讀取的腫瘤成像之外,由其所介導的智能光熱治療方法在精準殺滅腫瘤組織的同時,還能減少對於健康組織的傷害。
同時,在其他醫學領域比如心血管疾病、神經科學和免疫學等領域,iDNR 還有更多的套用潛力有待挖掘。
研究人員表示:「這些套用前景還需要時間和後續研究的驗證,但是這項技術的創新性和潛力,很有希望讓其成為腫瘤診斷和腫瘤治療的重要方向之一。」

當前的腫瘤診斷技術有何瓶頸?
據介紹,在腫瘤定位、手術引導和預後監測中,腫瘤成像扮演著至關重要的角色。隨著生物納米技術的發展,光熱成像、光聲成像、核磁共振成像、多模態成像等腫瘤診斷技術陸續得到發展。
然而,在特異性以及成本效益這兩方面,上述幾種技術依然存在以下兩種限制:
其一,在使用這幾款技術的時候,會出現非智能的「始終開啟」或輸出單參數響應訊號的情況,以至於很難將腫瘤組織訊號和正常組織背景進行區分;
其二,對於磁共振成像、正電子發射斷層掃描等現有腫瘤診斷策略來說,不僅成本較高而且需要大型器材。
也就是說,一款理想的腫瘤成像診斷策略,不僅要具備特異性的特點,還得擁有智能易讀的優勢,更得具備造價經濟便宜的特點。
那麽,這種理想策略為何遲遲無法面世?這是因為現有訊號分子的治療功能依然有限,導致很難以易於讀取的方式實作在體腫瘤成像和精確治療。
光熱材料,是一種能把紅外輻射轉化為熱能的材料。對於突破成像和治療的界限來說,它被認為是一種理想選擇。
由於透過紅外溫度計即可獲取光熱訊號,因此可以輕松地讀取數據,從而避免使用既耗時、又昂貴的儀器。
同時,光熱效應還具備殺死腫瘤細胞的特殊本領。但是,此前的光熱療法策略,往往存在非智能或單參數響應的問題,會導致腫瘤殺傷出現錯誤。
而對於腫瘤組織和正常組織來說,它們在多個參數方面都存在顯著差異,例如它們在生物標誌物和微環境上都有著極大不同, 這種不同恰恰可以為實作智能、精確的腫瘤成像和腫瘤治療,提供必要的前提條件。
此外,作為一類生物大分子,DNA 具備易於合成、可編程智能響應能力出色、化石相容性良好的特點。當為腫瘤成像和腫瘤治療制備智能納米材料的時候,DNA 是一種非常理想的選擇。
近年來,DNA 納米水凝膠、納米花、納米器件核酸生物材料,已經得到了學界的廣泛研究。當對 DNA 納米材料進行合理設計的時候,的確可以克服一些以往存在的難題。
但是,DNA 的一些其他缺點,比如穩定性差、在腫瘤組織中的靶向能力和保留能力差、難以智能地辨識腫瘤組織、以及難以獲取訊號等不足,依然尚未被攻克。為了解決這些問題,該團隊開展了本次研究。

實作簡單、易讀取的腫瘤成像
研究伊始,他們先是對現有腫瘤成像和治療技術的局限性,進行了全面的調研,透過此課題組了解到非常有必要實作簡單且易於讀取的腫瘤成像。
確定研究方向之後,他們開始進行概念構想與設計。考慮到該團隊的專長,他們決定使用核酸生物材料作為平台,並結合多價 AS1411 核酸適體和血紅素的概念。
在實驗驗證這一階段,課題組先是合成了核酸生物材料,然後開展了成像效果和治療效果的模擬實驗。
在設計方案得到初步驗證之後,他們針對所打造的體系進行多次最佳化和改進。後來,課題組又多次調整設計方案,透過嘗試不同的 DNA 結構、材料組合和操作條件,提高了 iDNR 的效能和選擇性。
在體外實驗驗證成功之後,他們又開始轉向動物模型,基於此開展動物體內試驗和效果驗證。
楊宇表示:「在將 iDNR 從體外試驗轉移到動物模型的過程中,我們嘗試了很多參數,也克服了體內環境的復雜性,以讓安全性和有效性得到確保。」
在動物模型上得到驗證之後,他們又將 iDNR 用於真實腫瘤的治療之中,以便評估 iDNR 在活體內的成像效果和治療效果。
在多次驗證成功並獲得充分數據之後,他們開始分析實驗結果,並將這一研究整理為論文。
在本次工作尚未結束之時,論文第一作者恰逢畢業季,正面臨找工作的人生大事。這時,該如何既讓第一作者順利畢業、又能確保論文如期發表?
好在整個團隊提前做好了規劃和溝通,針對論文預期發表時間和畢業時間線達成共識。
「可以說對於不可預見的情況,我們在做法上始終保持靈活性。同時在這個特殊的情況下,對於本次工作的圓滿完成,其他團隊成員也做出了重要貢獻。」楊宇說。

圖 | 課題組合影(來源:楊宇)
最終,相關論文以【智能 DNA 納米反應器,可實作易於讀取的體內腫瘤成像和精準治療】(An Intelligent DNA Nanoreactor for Easy-to-Read In Vivo Tumor Imaging and Precise Therapy)為題發在 Angewandte Chemie International Edition (IF 16.6)。

圖 | 相關論文(來源:Angewandte Chemie International Edition)
上海交通大學毛東升博士是第一作者,上海交通大學楊宇研究員和同濟大學附屬第十人民醫院朱小立研究員擔任共同通訊作者。

圖 | 楊宇(來源:楊宇)
未來,如何將 iDNR 這種智能核酸生物材料推向臨床轉化,是課題組的另一個重要目標。要想實作這一目標,就要在臨床前研究和動物模型上進行深入研究。
另外,他們將繼續探索和最佳化 iDNR 在腫瘤治療中的套用策略,包括將腫瘤光熱治療與免疫治療相結合,以便在提高治療效果的同時,也能降低潛在的副作用。
同時,他們還考慮結合不同的成像技術,比如結合光熱成像、光聲成像和核磁共振成像等技術, 進一步提高 iDNR 的成像精度和多模態成像融合的能力,從而實作更加全面的腫瘤檢測結果和腫瘤監測效果。
如果這些後續計劃能夠順利完成,其將進一步完善和發展基於 iDNR 的腫瘤成像和治療策略,從而在臨床實踐中發揮更大的作用。另據悉,目前該課題組正在招募博士後,有意者可郵件聯系 [email protected]
參考資料:
1.Mao, D., Dong, Z., Liu, X., Li, W., Li, H., Gu, C., ... & Yang, Y. (2023). Intelligent DNA nanoreactor for in vivo easy‐to‐read tumor imaging and precise therapy. Angewandte Chemie International Edition, e202311309.
營運/排版:何晨龍











