

在過去的二十年中,硼化已成為替代許多原料化學品中豐富非活性碳氫鍵的一種手段。氫原子轉移(HAT)過程可以克服惰性C(sp3)-H鍵的強鍵解離能(BDEs),從而將原料烷烴轉化為增值的精細化學物質。然而,HAT試劑的高反應性,加上不同的C(sp3)-H鍵強度之間的微小差異,使直鏈烷烴的位點選擇性轉化成為一個巨大的挑戰。
在此, 中山大學胡鵬教授等人 提出了一個在具有小空間位阻的襯底中光催化分子間自由基取樣過程,用於鐵催化的末端C(sp3)-H鍵的硼酰化,包括非支鏈烷烴。機理研究表明,該反應透過一個可逆的HAT過程進行,隨後是碳自由基的選擇性硼酰化,硼-亞碸配合物可能有助於所觀察到的高末端區域選擇性。
相關文章以「 Terminal C(sp3)-H borylation through intermolecular radical sampling 」為題發表在 Science 上。
研究背景
長期以來,化學家一直在尋求透過C-H鍵官能團化,高效且可持續地將非反應性原料烷烴轉化為增值精細化學品。過渡金屬催化作用的出現使得芳香族化合物中C(sp2)-H鍵和具有定向基團的受質中C(sp3)-H鍵的功能化取得了很大的進展。盡管如此,以選擇性的方式直接改性惰性烷烴仍然是一個主要的挑戰,只有少數使用貴金屬催化劑的開創性研究被報道。此外,C-H鍵對過渡金屬催化劑的反應性通常依賴於相應的鍵酸度(圖1A),末端炔烴和芳香環優先與烷烴片段反應,導致受質對C(sp3)-H鍵功能化的限制。
相比之下,C-H鍵對均解的活性主要依賴於鍵的解離能(BDE),其中C(sp3)-H鍵的BDE水平最低(圖1A)。因此,透過活化物質,C(sp3)-H鍵的裂解可以透過HAT(氫原子轉移)過程,使其與芳烴、烯烴甚至末端炔部份相容,而C(sp3)-H鍵被裂解形成烷基自由基以進行進一步反應。盡管HAT是各種化學、環境和生物過程中的一種基本機制,但傳統的HAT反應通常需要套用化學計量的HAT前驅體或苛刻的條件。在分子內,HAT策略已被用於包含可產生自由基的定向基團的基質,促進遠端C-H鍵的裂解。
然而,在溫和的條件下實作C(sp3)-H鍵的分子間均解通常需要使用高活性的HAT試劑,這通常表現出較低的區域選擇性,並導致產物混合物。C(sp3)-H鍵之間的BDE值的細微差異是選擇性較差的另一個原因,盡管在熱力學上,亞甲基或甲基由於其鍵強度較低,代表了首選的反應位點(圖1B)。為了解決這個長期存在的問題,一些巧妙的研究使用了具有C(sp3)-H鍵的受質,具有不同的空間位阻或不同的電子性質,以產生區域選擇性的C(sp3)-H功能化產物。然而,實作簡單烷烴的選擇性修飾,特別是非支鏈的末端功能化,是一個巨大的挑戰(圖1B)。
研究內容
本文考慮了兩種一般的途徑來解決使用正己烷作為模型分子的區域選擇性挑戰(圖1C)。第一個途徑涉及一個區域選擇性的HAT,然後是功能化。然而,由於前面所指出的困難,這一過程迄今為止只實作了適度的末端選擇性。作為一個例子,之前報道了空間受阻受質末端甲基選擇性硼化的開創性工作,該受質使用原位形成的氯自由基-硼「酸」配合物作為選擇性HAT催化劑。這種方法抽象了空間無阻礙的C(sp3)-H鍵,並實作了不尋常的選擇性。然而,當套用於直鏈受質(如戊烷)時,該系統表現出不令人滿意的區域選擇性。
第二種途徑從非選擇性HAT步驟開始,使初級和二級自由基的形成,然後是自由基采樣程式,以實作末端功能化產物的形成。非反應性次級自由基透過反向HAT反應恢復到受質分子(圖1C),當系統能夠根據空間位阻區分初級自由基和次級自由基時,這種策略似乎更可靠。氯化鐵(III)已被確定為一種很有前途的前驅體,用於透過光誘導配體到金屬電荷轉移(LMCT)過程生成氯自由基。

圖1. 透過HAT實作非支鏈烷烴中 C(sp3)-H 鍵選擇性的挑戰

圖2 . 簡單基底的範圍
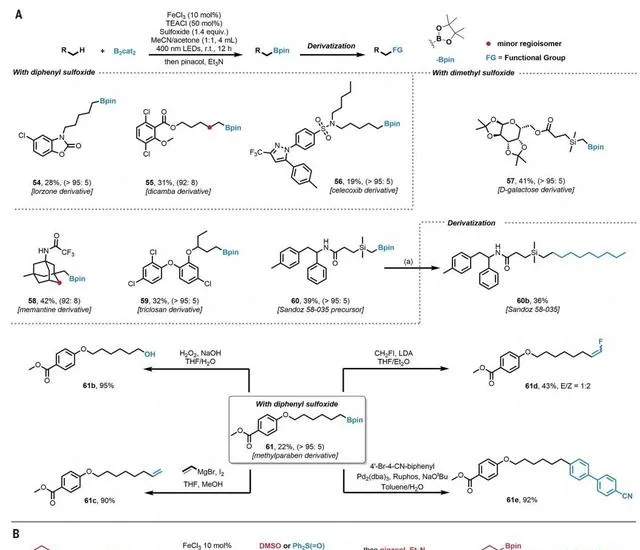
圖3 . 進一步的套用

圖4 . 機理研究
圖5. 機理的進一步提出
綜上,本文透過氯化鐵光催化實作了具有不同空間位阻的非支鏈烷烴和受質的區域選擇性端C(sp3)-H硼酰化。與傳統的金屬催化方法不同,該方法證明了在C(sp2)-H和C(sp)-H鍵上選擇性功能化C(sp3)-H鍵的能力,顯示出廣泛的官能團耐受性。該策略為透過HAT實作區域選擇性C(sp3)-H鍵功能化提供了一種簡單方便的方法,特別是對於具有小空間位阻挑戰性的受質。
Miao Wang, Yahao Huang, Peng Hu*, Terminal C(sp3)-H borylation through intermolecular radical sampling , Science (2024).











