本文來源:時代商學院 作者:畢肖磊

來源|時代商學院
作者|畢肖磊
編輯|鄭少娜
百濟神州(688235.SH)是A股知名創新藥企業,2017—2024年上半年,該公司各期研發投入在A股化學制藥公司(申萬二級)中均為最高,研發費用合計超600億元。
但對百濟神州而言,成立至今,持續虧損這一「達摩克利斯之劍」始終高懸。截至今年上半年末,該公司仍未實作盈利。9月20日,保薦機構釋出的持續督導報告稱百濟神州存在大額累計及持續虧損,未來可能被退市的風險。
時代投研研究發現,百濟神州存在的退市風險,主要為未來可能出現「明顯喪失持續經營能力」的各項情形,這與其創新藥產品銷售情況息息相關。而該公司巨大的研發投入並未取得預期效果,截至上半年末,該公司仍只有3款藥物獲批上市。
此外,百濟神州目前賴以生存的核心藥品澤布替尼在美國陷入侵權訴訟,經營或受影響;另一產品替雷利珠單抗市場競爭激烈,或難以復制澤布替尼的成功道路;從在審新藥品種來看,該公司短期內難以推出新藥上市貢獻營收。
9月26日—27日,就何時實作盈利、是否存在較大退市風險等問題,時代投研向百濟神州發函及致電詢問。截至發稿,對方仍未回復。
累計未彌補虧損超600億元,百濟神州或存退市風險
財報顯示,百濟神州是一家專註於創新藥研發、生產及商業化的公司,成立於2010年10月,成立至今,其虧損問題始終難解。2017—2024年上半年,百濟神州歸母凈利潤均為虧損狀態,這與其居高不下的期間費用密切相關。
據財報,如圖表1所示,2017—2024年上半年,百濟神州投入的研發費用共計622.76億元,銷售費用共計265.08億元,兩項費用合計占營收總和的比例為162.7%,且均呈持續增長態勢。
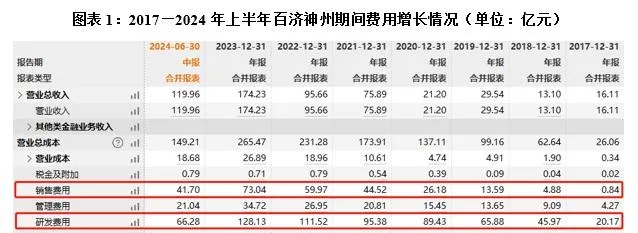
在2024年半年報中,百濟神州表示,其銷售費用同比增長22.4%,主要系全球商業化的持續投入所致;研發費用同比增長12.68%,則主要系隨著全球研發管線的擴張,臨床及臨床前候選藥物的研發投入增加所致。
但從結果來看,與同行相比,百濟神州的研發效率並不高。截至今年上半年末,百濟神州自主研發並獲批上市藥物只有澤布替尼、替雷利珠單抗、澤尼達妥單抗3款。
據半年報,同行公司中,同期君實生物(688180.SH)有3款創新藥產品在售;復星醫藥(600196.SH)有4款自主研發創新藥獲批上市;恒瑞醫藥(600276.SH)有13款已上市創新藥;上市僅1年的科倫博泰生物(6990.HK)也表示,今年下半年或明年上半年將有4款創新藥品上市。
如圖表2所示,2024年上半年,百濟神州投入的研發費用超過上述4家同行公司總和。
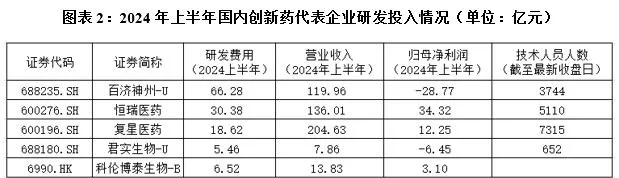
值得註意的是,在長期投入大量研發費用但產出結果不盡人意之後,百濟神州已因持續虧損面臨退市風險。
9月20日,中金公司(601995.SH)、高盛(中國)證券有限責任公司釋出督導報告表示,百濟神州存在大額累計及持續虧損,在可預見的期間記憶體在無法現金分紅且未來可能被上交所啟動退市程式的風險。
據【上海證券交易所科創板股票上市規則】,目前,百濟神州不符合重大違法強制退市或交易類強制退市情況,主要風險為財務類強制退市,具體包括主營業務大部份停滯或者規模極低、經營資產大幅減少導致無法維持日常經營等「明顯喪失持續經營能力」的各項情形。
因此,在需要保持持續高額研發投入的情況下,百濟神州能否保住上市資格,主要取決於其現有創新藥產品的經營情況,以及能否及時推出新產品以貢獻收入。
核心產品在美遭專利訴訟,新藥在審專案短期難貢獻收入
從現有產品來看,半年報顯示,今年上半年,百濟神州三款已上市藥品中,澤布替尼、替雷利珠單抗分別實作收入80.18億元、21.91億元,占該公司總收入的比例合計為85.1%。
可以看出,百濟神州對上述兩款藥品具有較大的經營依賴性。其中,貢獻近七成收入的澤布替尼主要收入來源為美國地區(銷售收入占比為73.62%),但該藥品目前在美國正卷入多起訴訟。
據半年報,2023年6月,美國藥企艾伯維(ABBV.US)旗下公司在特拉華州地方法院對百濟神州及其全資子公司提出申訴,聲稱百濟神州的澤布替尼產品侵犯自身一項於2023年6月13日獲授權的專利。
9月初,艾伯維在芝加哥聯邦法院對百濟神州提起訴訟,指控其非法盜取自身商業機密,用於開發針對血液癌癥的布魯頓氏酪胺酸激酶(BTK)降解劑專案(即澤布替尼產品)。
2024年3月8日,因仿制藥公司山德士、MSN公司向FDA(美國食品和藥物管理局)申請銷售百濟神州產品的仿制藥版本,百濟神州子公司向其提起專利侵權訴訟。
此外,在澤布替尼同時面臨知識產權訴訟和潛在仿制藥競爭之時,百濟神州另一款核心產品的前景也並不明朗。
2024年3月,百濟神州替雷利珠單抗產品在FDA的新藥上市申請獲批,該產品是一款用於治療多種實體瘤及血液腫瘤的抗PD-1抗體免疫療法,而PD-1賽道的市場競爭異常激烈。
目前,全球已有多款抗PD-1藥物被FDA批準上市,包括醫藥巨頭默沙東(MRK.US)的帕博利珠單抗、施貴寶(BMY.US)的納武利尤單抗等。其中,帕博利珠單抗上半年的銷售收入超過142億美元。
國內方面,據國家藥監局南方醫藥經濟研究所旗下【醫藥經濟報】,如圖表3所示,截至今年上半年,國內獲批上市的PD(L)-1單抗已達15款。
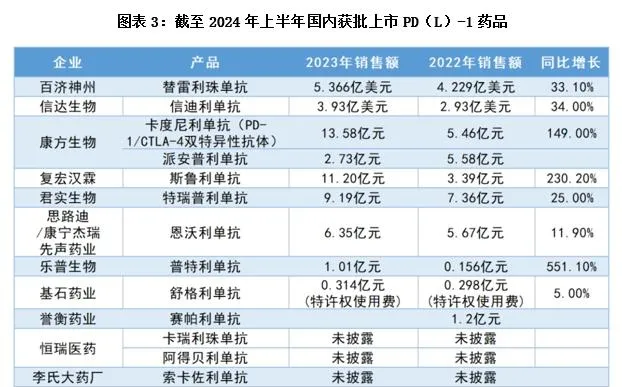
從新產品來看,半年報顯示,除已上市藥物新增適應癥之外,百濟神州進入臨床三期階段的新藥品種僅有4款。其中,據國家藥監局藥品審評中心,截至9月26日,在審新藥品種僅有Sonrotoclax薄膜包衣片一款。
據【藥品註冊管理辦法】,上市申請的常規品種審批程式為200個工作日。因此,百濟神州至少要等到明年二季度才有一款新藥貢獻收入,其能否幫助百濟神州度過經營危機,目前尚未可知。
(全文2229字)
免責聲明:本報告僅供時代商學院客戶使用。本公司不因接收人收到本報告而視其為客戶。本報告基於本公司認為可靠的、已公開的資訊編制,但本公司對該等資訊的準確性及完整性不作任何保證。本報告所載的意見、評估及預測僅反映報告釋出當日的觀點和判斷。本公司不保證本報告所含資訊保持在最新狀態。本公司對本報告所含資訊可在不發出通知的情形下做出修改,投資者應當自行關註相應的更新或修改。本公司力求報告內容客觀、公正,但本報告所載的觀點、結論和建議僅供參考,不構成所述證券的買賣出價或征價。該等觀點、建議並未考慮到個別投資者的具體投資目的、財務狀況以及特定需求,在任何時候均不構成對客戶私人投資建議。投資者應當充分考慮自身特定狀況,並完整理解和使用本報告內容,不應視本報告為做出投資決策的唯一因素。對依據或者使用本報告所造成的一切後果,本公司及作者均不承擔任何法律責任。本公司及作者在自身所知情的範圍內,與本報告所指的證券或投資標的不存在法律禁止的利害關系。在法律特許的情況下,本公司及其所屬關線上構可能會持有報告中提到的公司所發行的證券頭寸並進行交易,也可能為之提供或者爭取提供投資銀行、財務顧問或者金融產品等相關服務。本報告版權僅為本公司所有。未經本公司書面特許,任何機構或個人不得以翻版、復制、發表、參照或再次分發他人等任何形式侵犯本公司版權。如征得本公司同意進行參照、刊發的,需在允許的範圍內使用,並註明出處為「時代商學院」,且不得對本報告進行任何有悖原意的參照、刪節和修改。本公司保留追究相關責任的權利。所有本報告中使用的商標、服務標記及標記均為本公司的商標、服務標記及標記。











