2013年5月,亞洲首例豬-猴異種異位部份肝移植獲得成功;2020年6月,異種肝移植受體存活重新整理世界紀錄;2023年,異種異位輔助肝移植取得新突破;2024年3月10日這一次,則首次將一只多基因編輯豬的全肝,以輔助的方式移植到一位腦死亡患者體內……至此,空軍軍醫大學西京醫院歷經11年的異種肝臟移植臨床研究,取得重大突破,豬肝有望很快用於移植挽救肝衰竭患者。
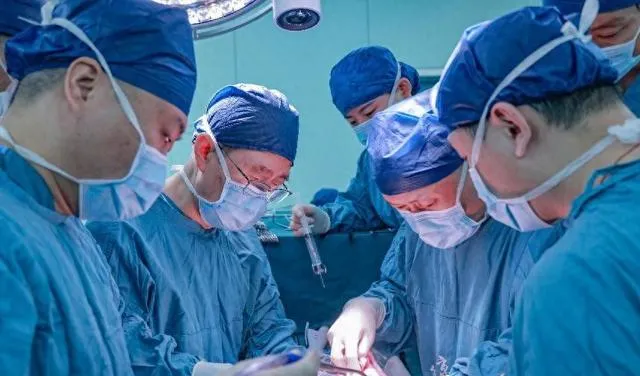
重大突破 豬肝首次被移植到人體內
3月10日,對陜西乃至全國來說,都是值得銘記的日子。因為這一天,中國科學院竇科峰院士、空軍軍醫大學西京醫院陶開山主任團隊,在多次的「豬猴異種肝移植動物實驗」基礎上,以成都中科奧格生物科技有限公司提供的一頭O型血、23公斤重的多基因編輯豬作為供體,一例重型閉合性顱腦損傷導致的腦死亡患者作為受體,實施了保留移植患者自身肝臟的輔助性肝移植,模擬了臨床肝衰竭患者的替代支持治療過程,屬世界首例。至此,異種肝臟異種移植步入臨床研究階段,該研究首次探索了「基因編輯豬-人」肝臟異種移植的可行性。
3月17日,記者從西京醫院了解到,3月10日手術當天,麻醉科、外科手術室、心血管外科等14個科室共同參與,一切準備就緒後,供體豬全麻,專家團隊開啟腹腔,遊離、灌註、獲取供肝,對供肝進行修整,稱重700g,組織學檢查顯示肝組織形態結構正常。受者常規麻醉,取腹部正中切口……術中,B超顯示移植肝灌註良好,整個手術歷時約9小時順利結束。
術後24小時,受體血流動力學平穩,移植肝臟膽汁分泌良好,B超顯示移植肝臟血供良好,移植肝臟穿刺病理顯示未見排斥反應。據西京醫院肝膽外科陶開山主任介紹,移植的基因編輯豬肝臟無論從膽汁、血供和病理結果來講,情況良好,手術效果超出團隊預想。
據竇科峰院士講,這是醫學界第一次將基因編輯豬肝植入人體內。目前,經超過96小時的觀察,移植的基因編輯豬肝臟,在人體內能夠發揮生理功能,正常分泌膽汁,說明有可能替代人類肝臟。
據了解,中國有近4億肝病患者,700多萬肝硬化患者,同時,每年新增30萬~50萬的肝衰竭患者。對於肝衰竭,肝移植是唯一有效根治方式。現實中,很多人因等不到人類供肝而失去生命。而被選擇為最佳供體的多基因編輯豬,因為其生理、生化與人體相似,易於基因改造、培育,繁殖周期短,可隨時獲得,而且數量不限,可使更多終末期肝病患者獲益,未來可能完全替代同種肝移植。
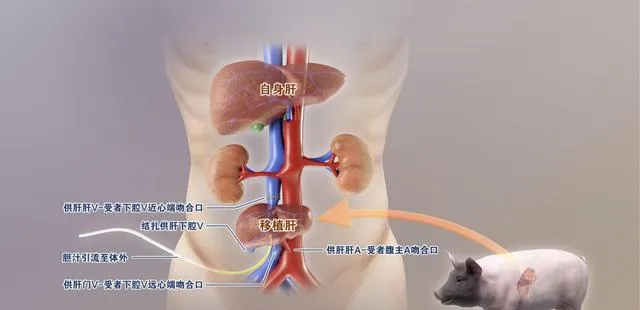
探索研究 豬-猴到豬-人移植歷經11年
記者采訪了解到,從2013年5月亞洲首例豬-猴異種異位部份肝移植獲得成功,到2024年3月的這次基因編輯豬至腦死亡受者肝移植,竇科峰院士、陶開山主任帶領的異種肝臟移植臨床研究團隊,為了能讓異種肝臟移植盡快運用於臨床,在長達11年的時間裏,先後進行了多次豬猴異種肝移植動物實驗。
2013年5月7日,成功完成國際首例轉基因豬-藏酋猴異種異位脾窩輔助性肝部份移植術,切除猴的脾臟,將豬的部份肝臟放在猴的脾窩。雖然手術很順利,但由於經驗不足,受體猴在存活26小時後不幸死亡。5月28日,開展了第二例同樣的移植實驗手術,手術切除受體猴的脾臟,將供體豬的200克肝臟放在猴的脾窩部位。截至2013年6月6日下午2時,移植豬肝的猴子,創下術後存活10天的最新醫學紀錄。
2020年6月13日,成功實施多基因編輯豬-猴肝心腎移植術,研究團隊將一個供體豬的肝、心、腎分別移植給3只恒河猴受體。期間,肝臟移植采用脾窩異位輔助性肝移植。術後,移植肝和受體存活超過16天,創造豬-猴輔助性肝移植受體存活世界紀錄。
2022年10月16日,歷時14個小時成功實施國際首例多基因編輯豬-猴多器官多組織同期聯合移植。研究團隊透過獲取1頭多基因編輯豬的肝臟、心臟、腎臟3個臟器,以及角膜、皮膚、骨骼3個組織,分別為4只受體猴同期實施肝腎聯合移植、心臟移植、角膜和皮膚移植、骨骼移植。術後,受體猴及肝臟等移植器官、組織存活良好。
2023年10月29日至30日,成功實施的多基因編輯豬-猴異位輔助肝移植,取得新突破。術中將1只基因編輯豬的肝臟、腎臟、心臟、腹壁、角膜、骨、神經等多個器官和組織,移植給7只受體猴,術後肝臟等器官功能良好。
2024年3月10日這一次,則首次將一只多基因編輯豬的全肝,以輔助的方式移植到一位腦死亡患者體內,且已持續工作超96小時。對此,竇科峰院士表示,該項研究的順利開展,是異種器官移植領域的重大突破,也是異種肝移植向臨床邁進的關鍵一步,為下一步的臨床套用提供了理論依據和數據支撐。
臨床套用 可暫時替代同種肝移植輔助治療
11年時間,歷經了多次豬猴異種肝移植動物實驗,此次進行的「基因編輯豬-人」肝臟移植,受體為何選擇腦死亡患者而非需要肝移植的肝衰竭患者?
據竇科峰院士介紹,異種器官移植采用狒狒、獼猴等動物作為移植受體,是進行臨床前研究所必需的,因為它們的結構和生理與人類最相近。對於以狒狒、獼猴為受體的異種移植,敲除了某些豬抗原的六基因編輯豬,可能會加重移植肝臟的排斥反應,但對以人體為受體的移植手術來說,卻是有益的。因此,采用腦死亡受體進行異種器官移植臨床試驗,能更好地反映移植器官的功能,檢測豬的基因編輯策略是否合適,也能積累更多臨床經驗。
另外,采用狒狒、獼猴等動物進行異種器官移植研究,往往會使用一些還處於研究階段的新型免疫抑制藥物,這些藥物沒有實作臨床套用,並不能直接用於疾病治療。因此,動物研究中最佳化的免疫抑制方案,並不一定適合人類受體。但以腦死亡患者為移植受體,則可使用臨床免疫抑制藥物,繼而得出最佳化的臨床異種器官移植免疫抑制策略。
「基因編輯豬-人」肝臟移植的成功實施,是否預示著豬的肝臟可替代人類肝臟發揮功能?
對此,竇科峰院士告訴記者,相對於腎臟和心臟,肝臟涉及合成、分解、凝血、解毒和免疫等功能,解剖結構和生理功能更為復雜,因此,基因編輯豬的肝臟還不能完全替代人類肝臟發揮功能,異種肝臟移植技術難度和科學意義更大。
盡管動物研究中,異種肝移植受體的存活時間沒有異種腎臟和心臟移植存活時間長,卻有著非常迫切的臨床急救需求。特別是對於急性暴發性肝功能衰竭患者,肝移植是唯一救命方式。因此,現階段將異種肝移植作為一種暫時的同種肝移植替代治療手段,或讓患者自身肝臟經過移植肝的幫助後功能得以恢復。從這個層面來講,異種肝移植就有非常大的臨床套用價值,這是該研究采用輔助性肝移植方式的原因。 (記者 李海濤)











