電子供體-受體復合物(EDA complex)具有無需額外光敏劑、轉化率高、環境友好等優勢,近年來在構建具有挑戰性的C-X (X = C,N,O,S,P) 鍵的反應中取得了重要進展。這其中,N-吡啶鹽類化合物憑借其本身的缺電子特性而廣泛作為EDA復合物的電子受體參與反應,從而實作高效C-C、C-B或C-S鍵構建以及吡啶的區位選擇性官能團化修飾(圖1A&B)。此外,蘭州化物所蘇毅進研究員透過N-吡啶鹽與極性不飽和化合物的[3+2]環化反應,巧妙地將缺電子的吡啶鹽原位轉化為富電性的[3+2]去芳構化的烯胺結構中間體,從而與分子內吸電子基組成相應EDA復合物,實作了光誘導的吡啶C-2位官能團化修飾,為此類化合物的綠色高價值轉化提供了新方法(圖1C)。另一方面,4-氮雜吲哚啉結構廣泛存在於具有生物活性的分子中,是一類重要的骨架分子(圖1D)。然而,相較於其廣泛的生理活性,針對此類化合物的合成手段卻嚴重依賴分子內環化反應,使得構建和拓展該類分子骨架十分困難,大大制約了對這類化合物藥學和生物學功能的進一步研究和利用。
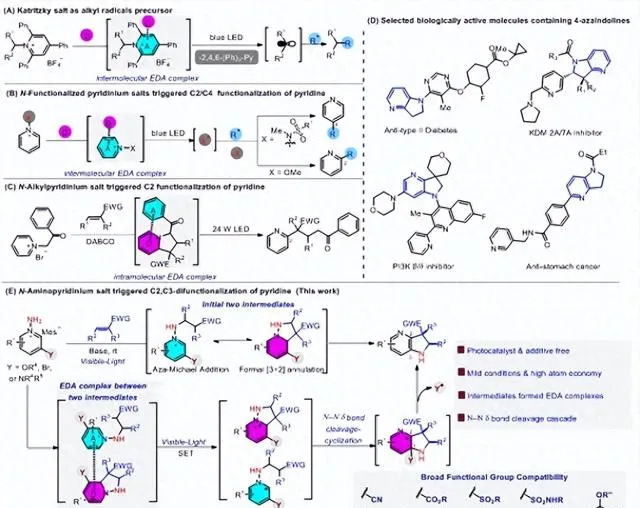
圖1. N-吡啶鹽參與的EDA復合物在有機合成中的套用
中國科學院成都生物研究所馬小鋒課題組一直致力於溫和條件下雜環化合物的合成與轉化方面的研究(Nat. Commun., 2020, 11, 914; Org. Lett., 2022, 24, 1454)。近期,該課題組發展了3-位具有供電子基修飾的N-胺基吡啶鹽與極性不飽和化合物在堿作用下,分別發生[3+2]環合反應以及Aza-Michael反應,形成富電性的共軛二烯胺中間體與缺電性的N-胺基吡啶鹽類中間體,兩者組成EDA復合物,繼而在光照下引發N-N鍵斷裂、N-遷移重排、芳構化串聯過程,高效、高區位選擇性地實作了吡啶C-2、C-3位雙官能團化修飾方法(圖1E)。該方法首次利用廉價易得的N-胺基吡啶鹽與極性不飽和化合物得到了結構多樣的4-氮雜吲哚啉,克服了以前僅能透過構建復雜吡啶前體繼而在相對劇烈或者重金屬催化下發生分子內環化反應構建此類結構的弊端。並且,此反應在實驗室常規熒光燈、LED白光或日光照射下均能以較高收率獲得目標產物,進一步展示了此反應的實用價值。此外,該方法不僅可以在克級規模制備4-氮雜吲哚啉類化合物,而且可以對一系列藥物或天然產物進行結構修飾。

圖2. 受質普適性研究
為進一步證明此方法的普適性,作者在最優條件下考察了受質的適用範圍(圖2)。研究表明,此反應對氰基、酯、碸、磺醯胺、鹵素、烯烴等官能團均表現出較好的耐受性,以中等到優秀的產率得到4-氮雜吲哚啉類化合物42個。其中,化合物4b的結構得到了晶體驗證。
為進一步考察此方法區位選擇性優勢,作者設計了具有占位基團的N-胺基吡啶鹽8與極性不飽和化合物在標準條件下反應,均以中等以上收率得到具有相反區位選擇性的4-氮雜吲哚啉分子12個(圖3)。其中,將9a與9c利用Ts保護後,成功得到了相應晶體,進一步確證了此類產物的結構。

圖3. 受質普適性研究
為了對反應歷程有更加深刻的理解,作者設計了一系列控制實驗,並根據實驗結果,提出了可能的反應機理(圖4)。最後,作者還透過密度泛函理論計算考察了此機理的能量水平,進一步驗證了提出機理的合理性。

圖4. 反應機理研究
文章來自中國科學院成都分院網站,如有侵權,請聯系刪除











