你可知道?毒胶囊中主要有毒成分是什么,今天我们要讨论就是它-镉。一种常见的对人体具有毒性的重金属。毒胶囊中有毒的主要成分就是胶囊壳中含有超过20ppm(药典)的镉元素。人类对镉元素的认识历程可以追溯到1817年,当时德国化学家弗里德里希·斯特罗姆耐尔在分析一批氧化锌时,意外地发现了镉元素。他将这种新元素命名为「镉」,因为它是从锌矿石中分离出来的,与锌相伴生。随着时间的推移,人们逐渐认识到镉对环境和人体健康的危害。例如,镉污染会导致土壤和水体受到污染,影响农作物和野生生物的生长和生存。此外,长期接触镉也会对人体健康产生负面影响,如引发肾脏、肺部和骨骼等方面的疾病。另外镉元素易在水稻,小麦中富集,是粮食中的重要监测项目之一。镉渡层呈现很好的金属光泽,在电镀行业也应用很广。下面我们来详细介绍一下这个元素。

镉元素的应用领域
镉(Cd)是一种化学元素,其化学符号为Cd,原子序数为48。它是一种质地坚硬、有光泽的银白色金属,具有良好的延展性。以下是镉元素在不同应用领域中的详细介绍:
电池:镉和镉化合物在镍镉电池中广泛应用。镉作为一个阴极材料,在电池中发生反应,提供了高能量密度和长寿命的电源。
光学器件:镉化合物在光学器件中起到重要作用。例如,镉硒(CdSe)和镉硫(CdS)等化合物可以用于制造光电二极管、激光器、太阳能电池等。
电子元件:镉在电子元件中也有广泛应用。例如,镉锌碲(CdZnTe)等化合物可用于制造半导体器件,如X射线探测器和核辐射探测器。
颜料:镉化合物常被用作颜料,具有艳丽的颜色和良好的耐光性。其中最常见的就是镉黄(CdS)和镉红(CdSe)。
防腐剂:镉镀层具有良好的耐腐蚀性,因此广泛应用于金属的防腐处理。
电子器件:镉作为半导体材料,也被应用于太阳能电池、光电二极管等电子器件中。
合金:镉可以与其他金属形成合金,如镉镀层钢和镉镉铅合金。这些合金具有耐腐蚀性和高温强度,被广泛用于汽车制造、航空航天等领域。
需要注意的是,镉是对环境和人体健康有害的物质。由于其毒性,对镉的使用和处理需谨慎,要遵循相关的环境和安全规定。

镉元素的物理性质
镉(Cd)是一种化学元素,呈现银白色,其物理性质如下:
相态:镉在常温常压下为固态。它具有金属特性,呈银白色。
密度:镉的密度较高,约为8.65克/立方厘米。这使得镉具有一定的重量和质感。
熔点和沸点:镉的熔点较低,约为321.1摄氏度(610.0华氏度),使其易于熔化和加工。而镉的沸点较高,约为767摄氏度(1413华氏度)。
导电性:镉是良好的导电体,具有较高的电导率。这使得镉在电子器件中具有广泛应用。
磁性:镉具有铁磁性,即在一定温度范围内会显示出磁性。然而,当温度超过特定临界值(约为13.2摄氏度)时,镉会变成顺磁性。
膨胀系数:镉的膨胀系数较大,即当温度升高时,镉的体积会扩大。这需要在设计和制造中考虑到其热膨胀性质。
硬度:镉的硬度较低,约为2.0摩氏硬度。因此,镉较容易被加工和成型。

镉元素的化学性质
镉其化学性质如下:
反应性:镉是一种活泼的金属,与大多数非金属元素发生反应。它可以与氧气、硫、卤素等元素反应,形成相应的化合物。
溶解性:镉在酸性条件下溶解性较好,例如在盐酸(HCl)或硝酸(HNO3)中能够溶解。而在碱性条件下,镉则不容易溶解。
氧化性:镉具有两个常见的氧化态,+2和+1。其中,+2氧化态是最常见的,称为二价镉。它可以通过与氧气反应,形成二氧化镉(CdO)等氧化物。
与非金属元素反应:镉与卤素(氟、氯、溴、碘)反应可以形成相应的卤化物,如氯化镉(CdCl2)。镉还可以与硫反应,形成硫化镉(CdS)等化合物。
腐蚀性:镉在湿气和氧气的存在下,会发生腐蚀。在空气中,镉表面会形成一层氧化镉(CdO)的氧化膜,从而减缓进一步的腐蚀。
合金性:镉可以与其他金属形成合金,如与铅形成合金(称为锡镉合金)。这种合金常用于电池、焊接和防腐等应用中。
需要注意的是,镉是一种有毒金属,其化合物对人体和环境具有危害。在使用和处理镉及其化合物时,需要遵循相关的安全操作规定和环境保护要求,以最大限度地减少对健康和环境的危害。
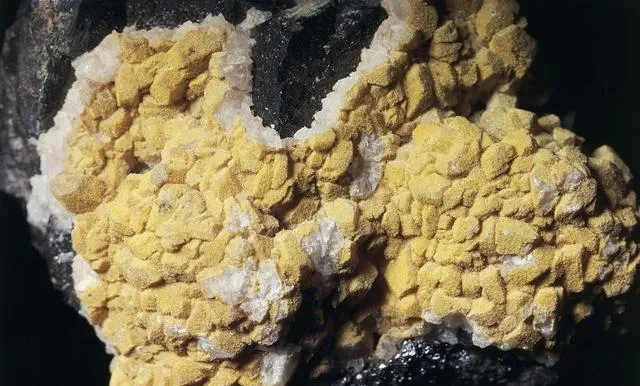
镉元素的生物特性
镉(Cadmium)是一种重金属元素,其在生物体内的生物特性引起了广泛关注。以下是镉元素的主要生物特性的详细介绍:
1. 吸收: 镉可以通过多种途径进入生物体内,包括食物、水和空气。在植物中,镉通过根部吸收,然后在食物链中逐渐富集。
2. 分布: 一旦镉进入生物体,它会在体内分布到各个组织和器官。镉在肝脏、肾脏、骨骼和肺中的富集较为显著。肾脏是镉积累的主要器官,因为镉主要通过肾脏排出体外。
3. 代谢: 镉在体内的代谢相对缓慢,主要以两价离子形式存在。在体内,镉主要以金属结合蛋白形式存在,其中金属硫蛋白是一种主要的结合物。
4. 排泄: 镉主要通过尿液排泄,尤其是通过肾脏。排泄速度相对较慢,导致镉在体内的蓄积。
5. 对骨骼的影响: 镉可以替代钙进入骨骼,导致骨骼中的钙被逐渐替代,从而影响骨骼的结构和稳定性。这可能导致骨质疏松和骨折的风险增加。
6. 对肾脏的影响: 镉对肾脏有较大的毒性,尤其是对肾小管的损害。慢性暴露于镉可能导致慢性肾脏疾病,并最终发展为肾功能衰竭。
7. 癌症风险: 镉被国际癌症研究机构(IARC)评估为对人类可能致癌的物质。长期暴露于较高浓度的镉可能与一些癌症,特别是肺癌和前列腺癌,有关。
8. 对生殖系统的影响: 镉可能对男性和女性生殖系统产生不良影响,包括降低生育能力和影响妊娠的结果。
9. 神经毒性: 镉的神经毒性效应也受到关注,尤其是在长期或高剂量暴露情况下。
由于这些生物特性,尤其是其对肾脏和骨骼的毒性,人们对于避免过量摄入和暴露于镉的关注日益增加。控制工业排放、合理用水、选择低镉含量的食品等措施都是减少镉暴露的方法。
镉元素的自然分布
镉(Cd)在自然界中以极微量的形式存在,并且很少以纯金属的形式出现。以下是镉在自然界中的分布情况:
地壳中含量:镉是地壳中的一种稀有元素,其平均含量约为0.1毫克/千克。尽管在地壳中的含量较低,但它在一些矿石中存在,如锌矿、铜矿和铅矿中。
矿石中富集:镉通常与其他金属元素共生于矿石中。最常见的镉矿石是锌矿石中的锌矾石(Sphalerite),其中可以含有可观的镉含量。此外,镉还可以与铅和铜矿石中的氧化物、硫化物和碳酸盐等形成矿石。
水、土壤和植物中的存在:镉可以通过天然过程进入水体和土壤中。它可以从岩石、矿石和土壤中被溶解或释放出来,然后被吸附到土壤颗粒中。镉也可以通过人类活动(如工业排放、农药使用等)进入水体和土壤中。一旦进入土壤,镉可以被植物吸收,并进入食物链中。

镉元素的开采提取及冶炼
镉的开采和冶炼提取主要有以下步骤:
矿石勘探:首先需要进行矿产资源勘探,寻找含有镉的矿石矿床。常见的含镉矿石主要是锌矿石中的锌矾石(Sphalerite),以及铅、铜等矿石中的氧化物、硫化物和碳酸盐。
采矿:确定了含有镉的矿床后,进行采矿操作。具体采矿方法根据矿床类型和地质条件的不同而有所差异,例如露天开采、井下开采或水文挖掘等。
破碎和粉碎:采矿后,将矿石进行初步破碎和粉碎操作,以减小矿石颗粒的大小。
高温冶炼:将矿石加热到高温,使其中的金属部分熔化。通过冶金过程,将矿石中的金属与其他杂质分离。在锌矿冶炼过程中,镉往往与锌一起提取,并通过不同的分离和提炼技术将镉分离出来。
电解:在一些冶炼工艺中,如电解过程,可使用电解池将金属离子还原为纯金属。在这一步骤中,将使用电流和适当的电解质处理以提取纯度较高的镉。
精炼和提纯:为了获得高纯度的镉,可能需要进行进一步的精炼和提纯步骤,例如真空蒸馏、气相色谱等。

镉元素的检测方法
镉元素的常用检测方式主要包括原子吸收光谱法、原子荧光光谱法、原子发射光谱法、电感耦合等离子体质谱法和X射线荧光光谱法。下面对这些方法进行详细介绍:
原子吸收光谱法(Atomic Absorption Spectroscopy,AAS):将样品溶液吸入火焰或石墨炉中,通过电热或化学反应使镉原子蒸发、激发、吸收特定波长的可见光,通过比较吸收光强度与标准溶液的差别来测定镉元素的含量。
原子荧光光谱法(Atomic Fluorescence Spectroscopy,AFS):将样品溶液通过喷雾、电化学或热解等方式产生镉原子蒸气,然后用激发光源激发镉原子,镉原子吸收能量后会发射特定波长的荧光,通过测量荧光强度来测定镉元素的含量。

发射光谱法(Atomic Emission Spectroscopy,AES):将样品溶液通过高频电磁场,火焰或电弧等方式将镉原子激发到高能级,在其回到基态时会发射特定波长的光线,通过测量这些光线的强度来测定镉元素的含量。
电感耦合等离子体质谱法(Inductively Coupled Plasma Mass Spectrometry,ICP-MS):将样品溶液通过等离子体喷雾进入质谱仪,利用高温等离子体使样品中的镉原子与气体离子化,然后通过质谱仪对离子进行分析和计数,从而确定镉元素的含量。
X射线荧光光谱法(X-ray Fluorescence Spectroscopy,XRF):将样品用高能X射线照射,样品中的镉原子受到X射线的激发后会发射出特定能量的荧光信号,通过测量荧光信号的强度来测定镉元素的含量。
这些常用检测方式具有灵敏度高、准确度高、选择性好等特点,广泛应用于环境监测、食品安全、生物医学等领域中对镉元素的检测。不同的方法适用于不同样品类型和含量范围,选择合适的检测方法可以提高检测效果
选择合适的镉元素检测方法需根据具体样品类型、测定要求和镉的含量范围等因素进行综合考虑。

原子吸收法测量镉元素的具体应用
在元素测量中,原子吸收法具有较高的准确性和灵敏度,为研究元素的化学性质、化合物组成以及含量提供了有效的手段。
接下来,我们使用原子吸收法来测量镉元素的含量。具体的步骤如下:
制备待测样品。将需要测量的样品制备成溶液,一般需要使用混酸进行消解,以便于后续的测量。
选择合适的原子吸收光谱仪。根据待测样品的性质和需要测量的镉元素含量范围,选择合适的原子吸收光谱仪。
调整原子吸收光谱仪的参数。根据待测元素和仪器型号,调整原子吸收光谱仪的参数,包括光源、原子化器、检测器等。
测量镉元素的吸光度。将待测样品放入原子化器中,通过光源发射特定波长的光辐射,待测镉元素会吸收这些光辐射,产生能级跃迁。通过检测器测量镉元素的吸光度。
计算镉元素的含量。根据吸光度和标准曲线,计算出镉元素的含量。
以下是一款仪器测量镉元素用到的具体参数。

实际工作中需要根据现场具体需要和条件选择适合的测量方法。以上这些方法在实验室和工业中广泛应用于元素的分析和检测。
镉(Cd)
标准物:纯镉片或镉粒(99.99%)或优级纯CdSO4·8pO。
方法:准确称取1.000g镉后,溶于少量(1+1)HNO3中,用水准确定容至1L,此溶液中Cd浓度为1000μg/mL。避光保存于聚乙烯瓶中。
火焰类型:空气-乙炔,贫燃焰。
分析参数:
波长(nm) 228.8
光谱带宽(nm) 0.4
滤波系数 0.3
推荐灯电流(mA) 2
负高压(v) 317.50
燃烧头高度(mm) 5
积分时间(S) 3
空气压力及流量(MPa,mL/min) 0.20
乙炔压力及流量(MPa,mL/min) 0.05,1300
雾化器型号 WNA-1型吴氏金属套玻璃高效雾化器
线性范围(μg/mL) 0.01~1
线性相关系数 0.9994
特征浓度(μg/mL) 0.010
检出限(μg/mL) 0.002
RSD(%) 0.55
计算方式 连续法
溶液酸度 0.5% HNO3
测量表格:
|
序号 |
测量对象 |
样品编号 |
Abs |
浓度 |
SD |
RSD[%] |
|
1 |
标准样品 |
Cd1 |
0.001 |
0.000 |
0.0003 |
42.5730 |
|
2 |
标准样品 |
Cd2 |
0.050 |
0.100 |
0.0001 |
0.2803 |
|
3 |
标准样品 |
Cd3 |
0.146 |
0.300 |
0.0010 |
0.7146 |
|
4 |
标准样品 |
Cd4 |
0.230 |
0.500 |
0.0013 |
0.5552 |
|
5 |
标准样品 |
Cd5 |
0.329 |
0.700 |
0.0007 |
0.2193 |
|
6 |
标准样品 |
Cd6 |
0.448 |
1.000 |
0.0003 |
0.0724 |
校准曲线:
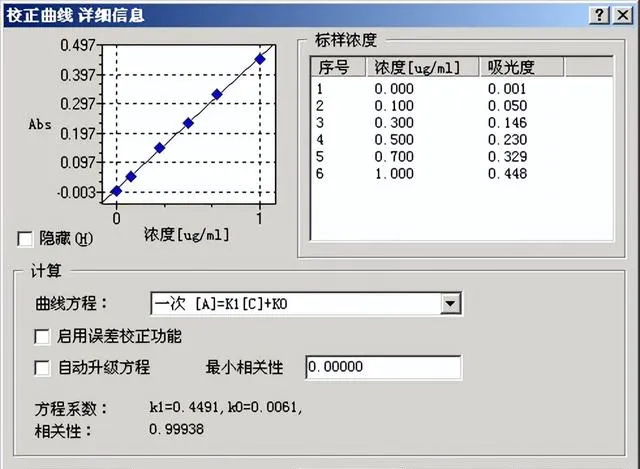
干扰:
在空气-乙炔火焰中未发现干扰。灯电流严重影响灵敏度,低的电流有高的灵敏度。火焰状态严重影响灵敏度,应仔细调节乙炔流量以获得最大灵敏度。
实际工作中需要根据现场具体需要选择适合的测量方法。这些方法在实验室和工业中广泛应用于镉元素的分析和检测。
镉元素是一个具有重要应用价值的元素,但同时也对环境和人体健康存在潜在的危害。随着科学技术的不断发展和环保意识的提高,人们需要更加深入地了解镉的性质和影响,采取有效的措施来限制其使用和排放,以保护环境和人类健康。虽然镉元素在现代社会中仍然发挥着重要的作用,但我们需要时刻警惕其潜在的危害,积极寻求更加环保和可持续的替代品,为未来的可持续发展做出贡献。