
2024年諾貝爾生理或醫學獎得主維克多·安布羅斯和蓋瑞·魯弗肯
導讀:今年的諾貝爾獎再次將聚光燈投向了生命科學領域,表彰了兩位在基因調控基本原理方面有卓越發現的科學家——安布羅斯和魯弗肯,他們發現了microRNA。
這一發現不僅揭示了生命體如何精準地控制基因表現,從而塑造出復雜多樣的生物形態和功能,更為我們理解生命本質、探索疾病治療的新途徑提供了寶貴的線索。
深究科學 | 撰文
兩位miRNA發現者被授予諾獎
10月7日台北時間,2024年諾貝爾生理或醫學獎揭曉,獎項授予維克多·安布羅斯(Victor Ambros)和蓋瑞·魯弗肯(Gary Ruvkun)兩位學者,他們因發現微小核糖核酸(miRNA)及其在轉錄後基因調控中的作用而獲獎。這一發現對於理解基因表現調控機制具有重要意義,也為疾病的治療提供了新的思路。

事實上,遺傳資訊就像一本精密的劇本,從DNA轉錄成信使RNA(mRNA),再經由細胞內的蛋白質生產機器,將遺傳指令轉化為實實在在的蛋白質。這一過程,自20世紀中葉以來,已被多項基礎科學發現所揭示。
然而,盡管所有細胞都攜帶著相同的DNA遺傳資訊,我們的器官和組織卻由多種不同型別的細胞構成,它們各自表達著獨特的蛋白質組合。這一奇妙的現象,正是基因活性調控的傑作。
基因活性調控確保了每個特定型別的細胞都能啟用正確的基因集,從而執行其特定的功能。如肌肉細胞、腸細胞和不同型別的神經細胞,正是透過這一機制,才能各司其職,共同維持著生命體的正常運轉。
此外,基因活性還需不斷微調,以適應我們體內和外界環境的不斷變化。一旦這一調控機制出現偏差,就可能引發嚴重的疾病,如癌癥、糖尿病或自身免疫性疾病。因此,理解基因活性的調控機制,一直是數十年來科學研究的重要目標。
早在20世紀60年代,科學家就發現了一種名為轉錄因子的特殊蛋白質,它們能夠結合到DNA的特定區域,透過決定哪些mRNA被生產出來,從而控制遺傳資訊的流動。自那時以來,科學家已經發現了數千種轉錄因子,並一度認為基因調控的主要原理已經得到解決。

然而,1993年安布羅斯和魯弗肯發表了一項顛覆性的發現——miRNA,隨即開啟了一個全新的領域。當時安布羅斯和魯弗肯對不同細胞型別如何發育充滿了興趣,在他們的不斷努力何探索中,最終發現了miRNA。這是一種全新的miRNA分子類別別,這些分子在基因調控過程中扮演著重要的角色,不僅揭示了一個全新的基因調控原則,更證明了這一原則對於多細胞生物,包括人類在內的生命體系,具有重大的意義。

獲獎後,維克多與夫人的合影
如今,我們知道人類基因組中編碼著超過1000多種miRNA。這些微小的分子,以其獨特的方式,在基因調控的舞台上大放異彩,它們透過復雜的交互作用網路,精確地調控著基因的表達,從而影響著生物體的發育和功能。
從研究小線蟲到發現miRNA後,兩位學者被冷落了7年
20世紀80年代末,安布羅斯和魯弗肯是H. Robert Horvitz實驗室的博士後研究員。Horvitz後來於2002年與Sydney Brenner和John E. Sulston共同獲得了諾貝爾獎。Horvitz利用線蟲作為研究物件,揭示了器官發育和細胞程式化死亡是如何受基因調控的。
也正受到導師的影響,在這個實驗室裏, 安布羅斯和 魯弗肯研究了一種看似不起眼的1公釐長的秀麗隱桿線蟲(C. elegans),這種蟲子盡管體型微小,卻擁有許多與更大、更復雜的動物體內相同的專門細胞型別,如神經細胞和肌肉細胞,此外它具有壽命短、易於控制生長條件、通體透明、體細胞數目恒定且特定細胞位置固定等優點,使其成為研究個體發生、發育生物學、遺傳學以及神經生物學的理想模型。

安布羅斯和魯弗肯對控制不同遺傳程式啟用時間的基因非常感興趣,這些基因確保了各種細胞型別在正確的時間發育。他們研究了兩種突變體線蟲——lin-4和lin-14,這兩種線蟲在發育過程中遺傳程式的啟用時間上存在缺陷。他們希望能辨識出突變的基因並了解其功能。
在此前的研究中,安布羅斯已經證明lin-4基因似乎是lin-14基因的負調節因子。然而,lin-14活性是如何被阻斷的,當時仍不得而知。安布羅斯和魯弗肯對這些突變體及其潛在關系產生了濃厚興趣,並著手解開這些謎團。
離開Horvitz實驗室之後,安布羅斯在哈佛大學新建的實驗室裏對lin-4突變體進行了深入分析。透過系統的基因作圖,他成功複制了lin-4基因,並有了意外的發現。lin-4基因產生了一種異常短的RNA分子,這種分子缺乏編碼蛋白質的程式碼。這些令人驚訝的結果表明,來自lin-4這種小分子RNA負責抑制lin-14。那麽,這是如何工作的呢?
與此同時,魯弗肯在麻省總醫院和哈佛醫學院新建的實驗室裏,他研究了lin-14基因的調控機制。與當時已知的基因調控機制不同,魯弗肯發現並不是lin-14的mRNA產生被lin-4所抑制,調控似乎發生在基因表現過程的後期階段,即透過關閉蛋白質生產來實作。實驗還揭示了lin-14 mRNA中一段對於lin-4抑制其活性所必需的序列。
安布羅斯和魯弗肯比較了他們的發現,並共同探索,從而取得了突破性進展。他們發現,短的lin-4序列與lin-14 mRNA關鍵段中的互補序列相匹配。他們進一步實驗證明,lin-4 miRNA透過與lin-14 mRNA中的互補序列結合,從而關閉了lin-14,阻斷了lin-14蛋白質的產生,接著他們發現了一種新的基因調控原理,這種原理是由一種以前未知的RNA型別——miRNA介導的。這一結果於1993年在【細胞】雜誌上發表了兩篇文章。
然而,這一發表的結果最初在科學界幾乎沒有得到回應。盡管結果很有趣,但這種不尋常的基因調控機制被認為只是秀麗隱桿線蟲的一種特性,可能與人類和其他更復雜的動物無關。
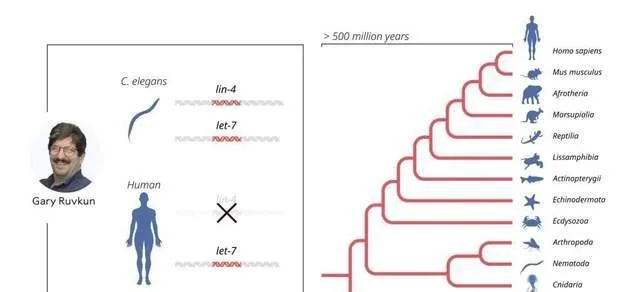
這種看法在2000年發生了改變,當時魯弗肯的研究小組發表了他們發現的另一種由let-7基因編碼的miRNA。與lin-4不同,let-7基因在整個動物界中高度保守。這篇文章引起了極大的興趣,在接下來的幾年裏,人們發現了數百種不同的miRNA。如今,我們知道人類體內有超過一千種不同的miRNA基因,並且miRNA介導的基因調控在多細胞生物中是普遍存在的。
miRNA如何進行基因調控
miRNA是一類重要的非編碼RNA分子,在基因表現調控中發揮著不可替代的作用。它們透過復雜的調控機制和精細的調控網路,實作對細胞生長、發育和疾病行程的精確控制。
miRNA的生物合成是一個復雜而精確的過程,它始於細胞核內的轉錄過程,主要包括編碼作用和非編碼作用兩種路徑。在編碼作用中,miRNA的結構被編碼在RNA聚合酶II轉錄的pri-miRNA中,經過加工形成預miRNA,再轉運至細胞質中,透過核酸酶和Dicer酶的剪下作用,最終生成成熟的miRNA。而在非編碼作用中,miRNA序列則存在於非編碼RNA的內含子或外顯子區域,透過內含子剪下或外顯子剪下的方式產生成熟miRNA。

很顯然,沒有miRNA的參與,細胞與組織無法正常發育。一旦miRNA的調控出現異常,便可能引發癌癥等嚴重疾病。編碼miRNA的基因發生突變,已在人類中導致先天性聽力損失、眼部及骨骼疾病等多種病癥。
此外,miRNA生產過程中的一種關鍵蛋白質發生突變,還會引發DICER1症候群,這是一種罕見但嚴重的疾病,與多種器官和組織的癌癥密切相關。
隨著研究的不斷深入和技術的不斷發展,我們有望對miRNA的調控機制和調控方式有更全面的認識,並探索出更多的針對性調控策略,為生命科學研究和醫學治療開辟新的篇章。
兩位諾獎得主簡介

安布羅斯是一位備受尊敬的美國發育生物學家,他於1953年出生於美國新罕布夏州的漢諾威,1979年獲得麻省理工學院(MIT)博士學位,1979年至1985年,安布羅斯在麻省理工學院進行博士後研究,期間積累了豐富的科研經驗和專業知識。
1985年,他成為哈佛大學的主要研究員,開始獨立領導科研計畫,並在該領域取得了顯著的成果。並在1992年至2007年期間擔任達特茅斯醫學院的教授。如今,他是麻薩諸塞大學醫學院自然科學領域的西爾弗曼教授。值得一體的是,一位華人學者Roselind Lee當年在安布羅斯實驗室讀博,參與了安布羅斯早年對miRNA幾乎所有的重要發現,後來這位優秀的學生,與安布羅斯喜結連理,成為名正言順的「科研贏家」。

魯弗肯則是一位在RNA調控領域做出傑出貢獻的科學家,他的研究成果不僅推動了生命科學的發展,還為人類理解生物體的基因表現、發育和疾病行程提供了新的視角和方法。
他於1952年出生在美國加利福尼亞州的柏克萊,1982年獲得哈佛大學博士學位,並在麻省理工學院從事博士後研究。1985年,他成為麻薩諸塞州總醫院和波士頓哈佛醫學院的主要研究員,現任遺傳學教授。
可以說,兩位學者在miRNA領域的原創性發現,不僅為我們開啟一扇理解基因調控的大門,還開啟了miRNA領域這個全新的研究領域,全球有無數分子生物學家從事這方面的研究,每年有成千上萬篇論文發表出來,為我們揭示生命的奧秘。
參考資料
1.The Nobel Prize in Physiology or Medicine 2024
2.https://www.nobelprize.org/prizes/medicine/2024/press-release/
3.剛剛,2024年諾貝爾生理或醫學獎揭曉!授予2位微小RNA及基因調控發現者 深究科學.
4.https://gruber.yale.edu/recipient/victor-ambros
5.https://gruber.yale.edu/recipient/gary-ruvkun
稽核:梁英 空軍軍醫大學第二附屬醫院藥劑科副研究員
出品:中國科協科普部
監制:中國科學技術出版社有限公司、北京中科星河文化傳媒有限公司












